Gaceta Parlamentaria, año XXVII, número 6633-I-2, miércoles 9 de octubre de 2024
- Que expide la Ley General del Cáncer, suscrita por el diputado Éctor Jaime Ramírez Barba y legisladores integrantes del Grupo Parlamentario del PAN
- Que reforma diversas disposiciones de la Ley Federal de Derechos y de la Ley General de Salud, en materia de fortalecimiento de la autonomía, el financiamiento de la regulación, control, vigilancia y fomento sanitario que realiza Cofepris, suscrita por el diputado Éctor Jaime Ramírez Barba y legisladores integrantes del Grupo Parlamentario del PAN
- Que reforma y adiciona diversas disposiciones de la Ley General de Salud, en materia de enfermedades raras, suscrita por el diputado Éctor Jaime Ramírez Barba y legisladores integrantes del Grupo Parlamentario del PAN
Que expide la Ley General del Cáncer, suscrita por el diputado Éctor Jaime Ramírez Barba y legisladores integrantes del Grupo Parlamentario del PAN
El que suscribe, Éctor Jaime Ramírez Barba, diputado del Grupo Parlamentario del Partido Acción Nacional, integrante de la LXVI Legislatura de la Cámara de Diputados del honorable Congreso de la Unión, con fundamento en lo dispuesto por los artículos 71, fracción II, y 72 de la Constitución Política de los Estados Unidos Mexicanos; 6, numeral 1, 77 y 78 del Reglamento de la Cámara de Diputados, somete a consideración de esta soberanía la presente iniciativa con proyecto de decreto por el que se expide la Ley General del Cáncer, al tenor de la siguiente
Exposición de Motivos
El cáncer en México es la tercera causa de muerte, por lo que está considerado como un problema de salud pública que debería ser prioritario por su magnitud y trascendencia, está relacionado con la transición demográfica y epidemiológica, el envejecimiento de la población y una mayor exposición a los factores de riesgo.
Desafortunadamente, durante este gobierno de Morena, la incapacidad en la gestión gubernamental del sector salud no ha permitido responder a las necesidades crecientes de detección oportuna y atención eficaz de los tumores malignos, lo que impacta negativamente la salud y expectativa de vida de las personas enfermas, así como el desarrollo de las familias, de la sociedad y el país.
En 2022, se registraron 89,574 defunciones por tumores malignos, la tasa de defunciones por esta causa aumentó de forma constante, al pasar de 62.04 defunciones por cada 100 mil personas en 2012, a 68.92 en 2022.1 En el futuro inmediato, las tendencias indican que una de cada tres personas tendrá un diagnóstico positivo de cáncer en 2025.2
Con el gobierno de la 4T, enfrentamos un serio retroceso en la atención médica a la que todas y todos tenemos derecho, le ha faltado capacidad e imaginación para superar las restricciones que representa el sistema de salud fragmentado que tenemos; no ha sido capaz de articular una política nacional que genere una atención homogénea en todas las instituciones del sistema para superar las inequidades y desigualdades que genera el mismo.
Este gobierno destruyó los avances que, aunque limitados, garantizaban una financiación de la atención de enfermedades prevalentes como el cáncer.
La falta de visión y planeación del actual gobierno no le ha permitido incrementar el personal capacitado para la detección oportuna del cáncer o especializado para la atención en los institutos nacionales o de los grandes hospitales donde se cuenta con atención especializada, generando condiciones de inequidad y desigualdad en el acceso a la atención médica de enfermedades altamente complejas, como los diferentes tipos de cáncer.
Hoy, un diagnóstico de cáncer en nuestro país representa para la mayoría de las familias el tener que enfrentar una serie de obstáculos para recibir una atención oportuna, pertinente y de calidad, dadas las insuficiencias que caracterizan actualmente a nuestro sistema público de salud.
No obstante, que en muchos casos el cáncer es un padecimiento prevenible, controlable y curable, desde el gobierno federal no se ha hecho lo necesario para instrumentar una verdadera política de prevención y promoción de la salud para que la población en general conozca los factores de riesgo y la necesidad de adoptar estilos de vida saludables.
Además, falta un esquema de educación continua para los médicos de primer contacto, a fin de que puedan identificar de forma oportuna signos y síntomas de sospecha o señales de riesgo para realizar la referencia oportuna correspondiente hacia a la atención especializada.
Nuestro país enfrenta el reto de adoptar estrategias preventivas oportunas, eficaces y de base científica, actualmente más del 70 por ciento de los pacientes con cáncer se diagnostican en etapas avanzadas, lo que reduce posibilidades de recuperación y supervivencia, además eleva los costos del tratamiento tanto de la familia como del sistema de atención pública.
Lamentablemente, como en otras políticas de salud, en la atención al cáncer vamos en retroceso; uno de los grandes desaciertos del actual gobierno fue eliminar al Seguro Popular y al Fondo de Protección contra Gastos Catastróficos, el cual contaba con más de 100 mil millones de pesos para garantizar la atención de enfermedades que ocasionan gastos catastróficos para las familias, entre ellas los diferentes tipos de cáncer.
Dicho Fondo se había venido constituyendo durante casi 15 años, sobre la base de un cálculo actuarial, que eventualmente permitiría ampliar la cobertura de un mayor número de padecimientos; sin embargo, el nuevo gobierno decidió destinar esos recursos a otros fines dejando desprotegidas a las miles de personas que desafortunadamente enfrentan un cáncer.
El saqueo de los recursos de este Fondo se ha traducido para quienes viven con cáncer en una tragedia; durante el actual gobierno se ha documentado recurrentemente la falta de atención médica especializada y de medicamentos oncológicos para niñas y niños, pero también para los adultos; a los cuales simplemente se les informa que no existe especialista disponible y que su cita tardará meses o que no hay medicamento y que tendrá que esperar y suspender su tratamiento o asumir el gasto de bolsillo que su adquisición representa.
Además, el gobierno de Morena desapareció el programa Seguro Médico Siglo XXI, que había contribuido de manera significativa a preservar la salud de todas las niñas y niños en el país, financiando la atención médica completa e integral de aquellos que no cuentan con ningún tipo de seguridad social. Con este programa niñas y niños beneficiarios recibían servicios de medicina preventiva y atención primaria a la salud, atención hospitalaria y de alta especialidad, incluidos los tratamientos contra el cáncer, a partir del día de su alta en el programa y durante la vigencia de sus derechos, sin desembolso por el servicio otorgado.
Solamente en 2019 se afiliaron al Seguro Médico Siglo XXI un total de 1,162,837 niños elegibles que, en conjunto, con el número de menores de cinco años de las familias afiliadas previamente al 2019, sumaban un total de 4.4 millones niñas y niños beneficiarios.3
En las reglas de operación del 2020 para este programa, las niñas y niños beneficiarios tenían garantizadas 151 intervenciones médicas, entre ellas: atención a leucemias, tumores renales, tumores del sistema nervioso central, tumores hepáticos, tumores óseos, linfomas, sarcomas y carcinomas. Pese a lo anterior, Morena desapareció el programa junto con el Seguro Popular.
Otra de las terribles decisiones de este gobierno en la lucha contra el cáncer fue el desmantelamiento del Registro Nacional de Cáncer.
Para poder identificar de mejor forma las necesidades de su atención a los diversos tipos de cáncer, el día 22 de junio de 2017, se reformó la Ley General de Salud para crear el Registro Nacional de Cáncer, con los siguientes objetivos:
1. Crear una red de registros
2. Orientar políticas públicas en prevención, detección temprana y tratamiento.
3. Contribuir en la planificación de servicios, infraestructura y adquisiciones.
4. Analizar la capacidad hospitalaria instalada.
5. Planear y garantizar la suficiencia de recursos humanos.
6. Planear y asignar recursos financieros.
Lamentablemente, la decisión del gobierno de Morena fue cancelar su integración, quitándole el presupuesto asignado por la Cámara de Diputados, por ello, el Registro Nacional de Cáncer está inoperante a partir de enero de 2021.
A través del registro podríamos conocer la situación real del cáncer en México con una planificación estratégica, algunos datos que podríamos conocer son: tasa de mortalidad, tasa de supervivencia, topografía, estudios y muchos otros datos que permitirían planear recursos humanos, financieros, de medicamentos y todo lo necesario para combatir al cáncer.
El Registro Nacional de Cáncer actualmente debería estar en etapa de consolidación, sin embargo, difícilmente lo logrará sin los recursos necesarios; además, es una obligación que tiene la Secretaría de Salud establecida en la Ley General de Salud, que contaba con el respaldo y colaboración de instituciones nacionales e internacionales como la Organización Mundial de la Salud (OMS), la American Cáncer Society y la Unión Internacional Contra el Cáncer. Contar con un registro sobre cáncer significa tener la información que permita conocer el comportamiento de la epidemiología de este grupo de padecimientos y permitirá planear una mejor atención médica y establecer medidas preventivas.
La atención del cáncer en el sistema público enfrenta la falta de especialistas, medicamentos y tratamientos de última generación o innovadores, diagnósticos más precisos con base en los nuevos desarrollos de la investigación científica en el campo de la medicina, y de la infraestructura adecuada y necesaria para controlar y lograr mayores tasas de éxito en el tratamiento.
Para ello, es necesario blindar los recursos públicos de las instituciones de salud que atienden tumores malignos, tenemos que replantear la forma en que se financia este tipo de padecimientos, de manera que se garantice un piso mínimo de recursos para las acciones de prevención, para el diagnóstico oportuno y para su tratamiento eficaz; además de lo necesarios para la investigación y la adopción de los nuevos desarrollos científicos y tecnológicos en el área médica.
Hoy necesitamos de una estrategia nacional que articule e involucre a todas las instituciones del sistema nacional de salud, con un enfoque centrado en las necesidades de los pacientes.
Por lo anterior, es necesario fortalecer las acciones para la detección temprana del cáncer, canalizar inmediatamente para su atención al paciente diagnosticado, en instituciones de atención médica especializada, mismas que deben contar con la tecnología más avanzada e incorporar los desarrollos de la ciencia genómica.
Se requiere de atención médica de calidad para garantizar a cada persona una atención oportuna, eficaz y de calidad contra el cáncer; así como, el acceso a medicamentos eficaces e innovadores que permitan restaurar su salud.
Tenemos que garantizar un sistema nacional de gestión y distribución de medicamentos oncológicos que permita surtir las recetas al 100% de forma oportuna, que garanticen el tratamiento indicado sin interrupciones ni cambios que los pongan en riesgo, a fin de brindar seguridad y tranquilidad a las y los pacientes y sus familias.
Priorizar la atención al cáncer mediante una estrategia nacional que asegure los recursos, acciones y las nuevas tecnologías y medicamentos innovadores para la atención de miles de pacientes, incluyendo niñas y niños que quedaron sin tratamiento debido a la eliminación de programas como el Seguro Popular y el Programa Seguro Médico Siglo XXI.
Se necesita reinstaurar y fortalecer el Registro Nacional de Cáncer para recopilar datos epidemiológicos clave; destinar recursos para su funcionamiento y consolidación, cumpliendo con la obligación establecida en la Ley General de Salud. Con lo anterior, podremos utilizar la información del registro para mejorar la atención médica, establecer medidas preventivas y planificar estrategias más efectivas en la lucha contra el cáncer en México.
También es necesario que en aquellos casos en los cuales el tratamiento curativo sea ineficaz, se cuente con la atención paliativa, esencial para mejorar la calidad de vida de los pacientes con enfermedad avanzada o terminal.
Otro aspecto importante es fortalecer la protección de la salud de las mujeres, atender las necesidades únicas de las mujeres, como el cáncer de mama, cáncer cervicouterino o cáncer de ovario.
El reto que enfrenta nuestro país en materia de atención al cáncer requiere de una visión renovada, que solo una nueva legislación logrará materializar acciones eficaces. Por ello, el proyecto de iniciativa que se presenta a consideración del Congreso tiene como objetivo, fortalecer el marco jurídico que fortalezca los mecanismos de atención integral del cáncer.
La iniciativa tiene como objetivo general establecer los mecanismos para garantizar la atención integral del cáncer como parte del derecho de protección a la salud establecido en el párrafo cuarto del artículo 4o de la Constitución Política de los Estados Unidos Mexicano; para toda persona con sospecha o diagnóstico de cáncer.
Señala que la atención integral del cáncer comprende: las pruebas diagnósticas para la detección oportuna de cáncer, la atención integral, completa y de calidad para paciente oncológico y los tratamientos y medicamentos innovadores; así como, a recibir las facilidades para acudir a diagnósticos preventivos o a los tratamientos de cáncer, sin que se vean afectados sus derechos laborales o salariales, entre otras.
Crea el Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer, como un mecanismo para la coordinación de las instituciones públicas, de seguridad social y privadas que otorguen servicios de prevención, atención y seguimiento a las personas con diagnóstico de cáncer; y faculta a la Secretaría de Salud para coordinar sus acciones.
Establece las facultades de dicho sistema nacional, así como las disposiciones su integración y funcionamiento.
Establece la Estrategia Nacional de Atención Integral al Cáncer, que tiene como objetivo señalar establecer las acciones gubernamentales que permitan disminuir la morbilidad y mortalidad ocasionada por los principales tipos de cáncer, la detección oportuna, el diagnóstico eficaz y referencia inmediata y articulada para un tratamiento especializado.
Señala las disposiciones para garantizar el financiamiento de las acciones de la Estrategia Nacional de Atención Integral al Cáncer; así como las que complementan la reactivación del Registro Nacional de Cáncer y los tratamientos y medicamentos innovadores para el cáncer como las nuevas tecnologías, que incluyen dispositivos médicos, o medicamentos biotecnológicos, con un efecto terapéutico mayor a las terapias y medicamentos existentes o comunes.
Lo anterior permitirá una acción gubernamental más eficaz para atender de manera integral a los diferentes tipos de cáncer; al coordinar de manera más eficiente las acciones y recursos del Estado mexicano en favor de quienes enfrentan este tipo padecimientos.
Es por lo anteriormente expuesto y fundado, que sometemos a la consideración de esta Soberanía, el siguiente proyecto de
Decreto por el que se expide la Ley General del Cáncer
Artículo Único. - Se expide la Ley General del Cáncer, para quedar como sigue:
Ley General del Cáncer
Capítulo I
Disposiciones Generales
Artículo 1 . La presente ley establece los mecanismos para garantizar la atención integral del cáncer como parte del derecho de protección a la salud establecido en el párrafo cuarto del artículo 4o de la Constitución Política de los Estados Unidos Mexicanos.
Sus disposiciones son de orden público, interés social y observancia general en el territorio nacional; su observancia será sin perjuicio de lo establecido en la Ley General de Salud y la Ley General para la Detección Oportuna del Cáncer en la Infancia y la Adolescencia y demás legislación aplicable.
Artículo 2 . Toda persona con sospecha o diagnóstico de cáncer tiene garantizado el derecho a la atención integral, de manera gratuita y prioritaria en los servicios públicos de salud, la cual debe incluir estudios y análisis clínicos, diagnóstico, tratamientos y medicamentos innovadores; así como acceso a los servicios de cuidados paliativos y medicamentos para el dolor.
Artículo 3 . El derecho a la atención integral del cáncer señalado en el artículo anterior comprende, de manera no limitativa, lo siguiente:
I. Las pruebas diagnósticas para la detección oportuna de cáncer deberán realizarse periódicamente a las personas que cumplan con los criterios de edad, sexo y factores de riesgo o que presenten signos o síntomas sugestivos de cáncer; mismos que deberán ser referidas inmediatamente para su confirmación diagnóstica y, en su caso, tratamiento;
II. La atención integral y completa del paciente oncológico por parte de personal de salud especializado y en instituciones acreditadas para servicios de salud oncológicos; así como, a recibir un trato preferencial en caso de urgencia;
III. Recibir los tratamientos y medicamentos necesarios, de acuerdo con las necesidades del paciente, entre los cuales se incluirán los tratamientos y medicamentos innovadores;
IV. Recibir un trato digno por parte del personal de salud responsable; así como, la información clara, oportuna, y veraz sobre su estado de salud y pronóstico esperado y los riesgos y alternativas de su tratamiento;
V. Cuando sea necesario, recibir las facilidades para acudir a diagnósticos preventivos o a los tratamientos de cáncer, sin que se vean afectados sus derechos laborales o salariales de conformidad con la legislación vigente, y
VI. Las demás que se establecen para los beneficiarios y los usuarios de los servicios de salud en la Ley General de Salud, la Ley General para la Detección Oportuna del Cáncer en la Infancia y la Adolescencia.
Capítulo II
De la Coordinación de los Servicios de
Atención integral
Artículo 4.- Se crea el Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer, como un mecanismo para la coordinación de las instituciones públicas, de seguridad social y privadas que otorguen servicios de prevención, atención y seguimiento a las personas con diagnóstico de cáncer.
Artículo 5 . La Secretaría de Salud, será la encargada de establecer y coordinar el Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer, para tal efecto emitirá los lineamientos correspondientes.
Artículo 6. Las instituciones del Sistema Nacional de Salud que brinden servicios de atención oncológica deberán participar en el Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer; así como, establecer los acuerdos o convenios para la referencia y contrarreferencia de pacientes, para garantizar la atención integral oportuna y de calidad para todas las personas con padecimientos oncológicos.
Artículo 7. El Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer se integra por los titulares de las instituciones de Sistema Nacional de Salud que otorguen servicios de atención a cáncer, el Sistema estará presidido por el titular de la Secretaría de Salud y contará con una secretaría técnica a cargo del titular del Instituto Nacional de Cancerología.
El Sistema se reunirá en sesión ordinaria una vez cada trimestre y en sesión extraordinaria, cuando sea convocada por la presidencia o por la mayoría de sus integrantes. Sus acuerdos se tomarán por la mayoría de los titulares integrantes del Sistema en la sesión correspondiente.
Por acuerdo del Sistema podrán participar en éste, con voz, pero sin voto, las instituciones académicas y de investigación, las sociedades científicas, asociaciones de pacientes, y profesionales expertos en temas oncológicos.
Artículo 8. El Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer, tendrá las facultades siguientes:
I. Participar en la elaboración y actualización del Programa Específico de Prevención y Control del Cáncer y de la Estrategia Nacional de Atención Integral al Cáncer en el marco del Programa Sectorial de Salud;
II. Participar en la elaboración de guías, protocolos y normas oficiales mexicanas de atención al cáncer;
III. Proponer acciones relacionadas con las mejores prácticas internacionales de atención del cáncer; así como la adopción de las tecnologías innovadoras para el diagnóstico y atención del cáncer;
IV. Establecer mecanismos para el seguimiento y evaluación de las acciones del Programa Específico de Prevención y Control del Cáncer y de la Estrategia Nacional de Atención Integral al Cáncer, así como las acciones de mejora;
V. Proponer la adopción de estándares de calidad para procedimientos de diagnóstico y tratamiento del cáncer basados en evidencia científica; así como, presentar propuestas para la adquisición de equipos médicos y tecnología innovadora para diagnóstico y tratamiento del cáncer;
VI. Colaborar en la integración y actualización del Registro Nacional de Cáncer que establece la Ley General de Salud;
VII. Promover la formación y capacitación continua del personal de salud en el diagnóstico y tratamiento del cáncer; así como la colaboración con instituciones de investigación para promover el desarrollo e innovación en el campo de la medicina oncológica;
VIII. Promover políticas de atención integral que considere los cuidados paliativos multidisciplinarios y la atención del dolor;
IX. Colaborar en la implementación de los modelos de atención de cuidados paliativos para enfermos terminales;
X. Establecer los mecanismos para la conformación de una red de instituciones de referencia y contrarreferencia oncológica a nivel nacional, regional o estatal, para facilitar el acceso a la atención integral;
XI. Promover, en cada institución, la integración de consejos técnicos multidisciplinarios e interdisciplinarios especializados en el diagnóstico y atención de los diferentes tipos de cáncer;
XII. Generar informes periódicos sobre el desempeño del Sistema, que incluya información y estadísticas sobre atención integral del cáncer, y ponerlos a disposición del público de forma transparente y accesible, y
XIII. Las demás que le otorgue la presente ley.
Capítulo III
De la Estrategia Nacional de Atención
Integral al Cáncer
Artículo 9 .- La Estrategia Nacional de Atención Integral al Cáncer, tiene como objetivo establecer las acciones gubernamentales que permitan disminuir la morbilidad y mortalidad ocasionada por los principales tipos de cáncer, la detección oportuna, el diagnóstico eficaz y referencia inmediata y articulada para un tratamiento especializado.
Debe integrar los mecanismos para fortalecer las acciones de prevención del cáncer a través de la promoción la adopción de estilos de vida saludable, de la alimentación saludable y la realización de actividad física, entre otros. Así como para la detección temprana, el diagnóstico oportuno y, en caso de confirmación, acceder al tratamiento inmediato y adecuado, atendiendo a las necesidades específicas de cada paciente.
Debe considerar también, el fortalecimiento de la infraestructura y equipamiento de las unidades de atención; así como las capacidades técnicas del personal de salud y el establecimiento de mecanismos de seguimiento y evaluación integral de las acciones y procesos, para la mejora continua de la Estrategia.
Artículo 10. La Estrategia señalará los mecanismos de coordinación de acciones entre las instituciones del Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer, para garantizar la atención integral del cáncer.
En los casos que sea posible, el seguimiento y control de los pacientes se podrá realizar mediante la atención domiciliaria o a distancia con apoyo de las nuevas tecnologías.
Artículo 11. La Estrategia debe considerar la inclusión y adopción de nuevas tecnologías, terapias, medicamentos e insumos innovadores para pacientes con cáncer; y en su caso, los tratamientos y medicamentos para el alivio del dolor y los cuidados paliativos.
Capítulo IV
Del Financiamiento para la Atención
Integral al Cáncer
Artículo 12.- Anualmente el financiamiento de las acciones de la Estrategia Nacional de Atención Integral al Cáncer, deberá considerarse por la Secretaría de Salud, el organismo Servicios de Salud del Instituto Mexicano del Seguro Social para el Bienestar (IMSS-Bienestar) y la Secretaría de Hacienda y Crédito Público en la elaboración del proyecto de Presupuesto de Egresos de la Federación que envíe el Ejecutivo federal a la Cámara de Diputados.
Artículo 13. - Además de los recursos señalados en el artículo anterior, se consideran los recursos del Fondo de Salud para el Bienestar, que establece la Ley General de Salud, destinados a la atención de enfermedades que impliquen un alto costo en los tratamientos y medicamentos asociados; parte de los cuales y de acuerdo con la demanda, se destinará a la atención integral del cáncer, compra de medicamentos oncológicos y demás insumos médicos relacionados.
Artículo 14.- La Secretaría de Salud o el organismo Servicios de Salud del Instituto Mexicano del Seguro Social para el Bienestar (IMSS-Bienestar), según corresponda, con cargo a su presupuesto, establecerá un mecanismo de reembolso para cubrir los gastos incurridos cuando un paciente oncológico no reciba la atención y medicamentos en el sistema público, y tenga que asumir el costo de los mismos, de acuerdo con los lineamientos que emitan al respecto.
Capítulo V
Del Registro Nacional de Cáncer
Artículo 15. Además de las disposiciones establecidas en la Ley General de Salud respecto del Registro Nacional de Cáncer, éste se integra de una base de datos que provee información consistente, completa, oportuna y de calidad sobre los casos de cáncer a nivel nacional y regional.
Artículo 16.- Las instituciones de Sistema Nacional de Salud que proporcionan u ofrezcan servicios de atención oncológica, están obligadas a proporcionar la información sobre los casos de cáncer necesaria para la integración y actualización del Registro Nacional de Cáncer.
Artículo 17.- La integración, coordinación y actualización del Registro corresponde a la Secretaría de Salud, misma que se auxiliará del Instituto Nacional de Cancerología para realizar las atribuciones que le corresponden en esta materia.
La Secretaría de Salud a propuesta del Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer, podrá establecer comités o grupos de trabajo que contribuyan a mejorar la operación, calidad de la información, efectividad y eficiencia del Registro.
La información estadística generada por el Registro se presentará semestralmente a través de los medios que determine la Secretaría de Salud; se presentará a nivel nacional y desagregada por entidad federativa, instituciones del Sistema Nacional de Salud, unidades médicas, tipo de tumor, sexo y grupo etario.
El Instituto Nacional de Cancerología publicará anualmente en su página de Internet, un informe que contendrá el acumulado de mortalidad e incidencia de casos de cáncer por región, así como el análisis específico de sobrevida.
La Secretaría de Salud emitirá el reglamento correspondiente para establecer las bases para la organización, integración y coordinación del Registro Nacional de Cáncer.
Capítulo VI
De los tratamientos y medicamentos
innovadores contra el Cáncer
Artículo 18.- Los tratamientos y medicamentos innovadores para el cáncer son las nuevas tecnologías, que incluyen dispositivos médicos, o medicamentos biotecnológicos, con un efecto terapéutico mayor a las terapias y medicamentos existentes o comunes.
Los tratamientos, medicamentos o dispositivos médicos para el cáncer deberán cumplir con todos los requisitos que establece nuestra regulación sanitaria; así como asegurar su eficacia, seguridad y calidad.
Artículo 29.- El Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer, solicitará la inclusión en el Compendio Nacional de Insumos para la Salud, de nuevas tecnologías, incluidos los dispositivos médicos, o medicamentos biotecnológicos contra el cáncer.
Artículo 20.- La Secretaría de Salud promoverá la investigación y desarrollo de tratamientos, terapias, medicamentos y dispositivos médicos innovadores contra el cáncer.
Capitulo VII
Disposiciones Finales
Artículo 21.- El incumplimiento de las disposiciones contenidas en la presente Ley será sancionado conforme a las disposiciones jurídicas aplicables, considerando la naturaleza y la gravedad del incumplimiento.
Transitorios
Artículo primero. El presente decreto entrará en vigor al día siguiente de su publicación en el Diario Oficial de la Federación.
Artículo Segundo. La Secretaría de Salud, en un plazo de ciento ochenta días contados a partir de la entrada en vigor del presente Decreto, deberá expedir los lineamientos para la integración y funcionamiento del Sistema Nacional de Coordinación de los Servicios de Atención al Cáncer, así como expedir y armonizar las demás disposiciones reglamentarias que correspondan, especialmente las relativas al Registro Nacional de Cáncer, conforme a lo dispuesto en el presente Decreto.
Artículo Tercero . La Secretaría de Salud en un plazo de ciento ochenta días contados a partir de la entrada en vigor del presente Decreto, deberá publicar la Estrategia Nacional de Atención Integral al Cáncer.
Notas
1 INEGI, Estadísticas a propósito del Día Mundial Contra el Cáncer, 2 de febrero de 2024. https://www.inegi.org.mx/contenidos/saladeprensa/aproposito/2024/EAP_CA NCER24.pdf
2 Juntos contra el Cáncer. Propuestas 2028-2024.http://juntoscontraelcancer.mx/jcc/wp-content/uploads/2018/05 /DOCPosicionamientoJCC2018.pdf
3 Acuerdo por el que se emiten las Reglas de Operación del Programa Seguro Médico Siglo XXI, para el ejercicio fiscal 2019. https://dof.gob.mx/nota_detalle.php?codigo=5551353&fecha=27/02/2019 #gsc.tab=0
Dado en el Palacio Legislativo de San Lázaro, a 9 de octubre de 2024.
Diputado Éctor Jaime Ramírez Barba (rúbrica)
Que reforma diversas disposiciones de la Ley Federal de Derechos y de la Ley General de Salud, en materia de fortalecimiento de la autonomía, el financiamiento de la regulación, control, vigilancia y fomento sanitario que realiza Cofepris, suscrita por el diputado Éctor Jaime Ramírez Barba y legisladores integrantes del Grupo Parlamentario del PAN
El que suscribe, Éctor Jaime Ramírez Barba, del Grupo Parlamentario del Partido Acción Nacional, y diputadas y diputados federales de la LXVI Legislatura, e integrantes del Grupo Parlamentario del Partido Acción Nacional, en ejercicio de la facultad de que otorgan los artículos 71 de la Constitución Política de los Estados Unidos Mexicanos; 6, numeral 1, fracción I, 77 y 78 del Reglamento de la Cámara de Diputados, somete a consideración de esta soberanía iniciativa con proyecto de decreto por el que se reforma la Ley Federal de Derechos y la Ley General de Salud, con el fin de fortalecer la autonomía, el financiamiento de la regulación, control, vigilancia y fomento sanitario que realiza Cofepris, al tenor de la siguiente
Exposición de Motivos
La salud es un valor fundamental en la vida de todo ser humano y una condición esencial para su desarrollo, así como uno de los pilares en los que cualquier Estado debe sustentar su crecimiento y estabilidad. En este sentido, la salud configura un derecho fundamental reconocido como tal en la Constitución Política de los Estados Unidos Mexicanos.
Derivado de las reformas constitucionales de 2011, se ha transitado de una definición tradicional sobre el derecho a la protección de la salud como un derecho social, de tipo programático, declarativo y sin carácter vinculante, hacia un derecho humano reconocido, con las implicaciones jurídicas que ello conlleva. Como consecuencia de lo anterior, el derecho a la salud ha evolucionado generando obligaciones a cargo de los poderes públicos con la finalidad de garantizarlo y hacerlo materialmente viable.
En este sentido, el Estado tiene la obligación de llevar a cabo acciones para garantizar y proteger la salud de las personas de manera que el derecho a la protección de la salud se pueda ejercer con plenitud y deje de ser sólo una aspiración.
Una de las principales responsabilidades del Estado es la protección de la salud a través de su política de protección contra riesgos sanitarios, y el ejercicio del control y fomento sanitario. La protección a la salud ha pasado por numerosas etapas a lo largo de la historia, en la cual se ha comprobado la importancia de prevenir en materia de salud, pues se reconoce que existe una estrecha vinculación entre la salud de la población, el desarrollo económico y su cohesión social.
En nuestro país, en la década de los ochentas se crea la Subsecretaría de Regulación y Fomento Sanitario que estaba integrada por cuatro Direcciones Generales: Medicamentos y Tecnologías para la Salud, Control Sanitario de Productos y Servicios, Salud Ambiental, Control Sanitario de la Publicidad, y el Laboratorio Nacional de Salud Pública; en esos años, se hicieron distintas modificaciones a la ley para buscar el mejor resultado de la Subsecretaría, con un enfoque de prevención, participación comunitaria y corresponsabilidad de los individuos como elementos fundamentales para alcanzar el objetivo de salud para todos.
Como parte de las respuestas ante la creciente importación de productos se creó en 1987 la Comisión Intersecretarial para el Control de Plaguicidas, Fertilizantes y Sustancias Tóxicas (Cicoplafest), para coordinar acciones en relación con la vigilancia y control de plaguicidas, fertilizantes y sustancias tóxicas. En ese año también, entraron en vigor 31 programas estatales de regulación sanitaria y se publicó el Reglamento de la Ley General de Salud en materia de Control Sanitario de Actividades, Establecimientos, Bienes y Servicios.
En junio de 1992, con la publicación de la Ley Federal sobre Metrología y Normalización, se transformó a las Normas Técnicas de Salubridad General, en Normas Oficiales Mexicanas (NOM), a fin de integrar todas las disposiciones a las que se sujetan tanto el gobierno como productores, proveedores de bienes y servicios y todos quienes se encuentran relacionados o interesados con las materias objeto de las NOM. En ese mismo año se instaló formalmente el Comité Consultivo Nacional de Normalización de Regulación y Fomento Sanitario.
En 1993, se modificó el Reglamento de Control Sanitario de la Publicidad y entre 1995 y 1996 se publicaron dos acuerdos regulatorios que determinaron el control de las áreas de mayor riesgo y se redujeron los trámites para las empresas. La generación de certidumbre se convirtió en uno de los factores fundamentales en esa etapa de regulación. En 1998 se publicó el Reglamento de Control Sanitario de Productos y Servicios.
Sin embargo, el tradicional modelo de regulación sanitaria empezó a mostrar síntomas severos de agotamiento ante la debilidad de varias de sus partes fundamentales como el desarrollo tecnológico, la infraestructura, la capacidad y la descoordinación operativa entre la Federación y los Estados. La aparición creciente de nuevos productos en el mercado cuya seguridad debía garantizarse y reforzarse la vigilancia de aquellos que ya se usaban o consumían, por lo que era necesario diseñar medidas y acciones para detectar y prevenir oportunamente los riesgos y daños a la salud.
Se buscó entonces integrar todas las funciones propias de la regulación y el fomento sanitarios en un solo órgano que unificará y diera homogeneidad a las políticas en la materia, es así es como nace la Comisión Federal para la Protección contra Riesgos Sanitarios, Cofepris.
Así el 5 de julio de 2001, se crea por Decreto Presidencial, la Comisión Federal para la Protección contra Riesgos Sanitarios como órgano desconcentrado de la Secretaría de Salud, con autonomía técnica, administrativa y operativa, que tiene a su cargo el ejercicio de las atribuciones en materia de regulación, control y fomento sanitarios en los términos de la Ley General de Salud y demás disposiciones aplicables.
Las funciones encomendadas a la Cofepris son articuladas con la operación de las entidades federativas a fin de integrar el Sistema Federal de Protección Sanitaria las cuales son: instrumentar la política nacional en materia de protección contra riesgos sanitarios; mejorar y ejercer la regulación, el control, la vigilancia sanitaria y la evaluación de riesgos a la salud derivados de los productos, actividades y establecimientos en materia de su competencia; y ejerce las atribuciones que actualmente tiene la Secretaria de Salud en materia de efectos del medio ambiente en salud, salud ocupacional, residuos peligrosos, saneamiento básico, accidentes que involucren sustancias tóxicas, peligrosas o radiaciones y sobre publicidad sanitaria.
A la Ley General de Salud se adicionó el artículo 17 Bis, mediante el cual la Secretaría señala que ejercerá, a través de la Cofepris, el control y vigilancia de los establecimientos a los que se refiere el artículo 3o fracciones I, en lo relativo al control y vigilancia de los establecimientos de salud a los que se refieren los artículos 34 y 35 de esta Ley, fracciones XIII, XIV, XXII, XXIII, XXIV, XXV, XXVI, y XXVII, ésta salvo por lo que se refiere a cadáveres que le confiere la Ley; y describe las atribuciones de la Comisión Federal.
El artículo 17 Bis 1, determina que la Comisión Federal, es un órgano desconcentrado de la Secretaría, contará con autonomía administrativa, técnica y operativa; y se describe cómo estará constituido su presupuesto.
El artículo 17 Bis 2, señala cómo se realizará la designación del titular del órgano desconcentrado. Además, se reformaron los artículos 313 y 340, por los cuales la Secretaría indica que, a través de la Comisión Federal, ejercerá el control sanitario de las donaciones y trasplantes de órganos, tejidos y células de seres humanos, así como de la disposición de sangre.
Con base en estas reformas a la Ley General de Salud, el 13 de abril del 2004, se publicó en el Diario Oficial de la Federación, el Reglamento de la Comisión Federal para la Protección contra Riesgos Sanitarios, mismo que derogó al decreto de su creación.
La creación de la Cofepris abrió paso a un proceso de transición de la regulación hacia la protección contra riesgos sanitarios, sustentado en evidencia técnica y científica en acciones orientadas a reducir o evitar enfermedades y muertes prevenibles; se le dotó de las herramientas jurídicas, a fin de tener las atribuciones y las competencias necesarias para cumplir la misión con estricto apego a la ley; innovar e implementar nuevos programas y estrategias que garanticen acciones sustantivas y mejoras continuas que protejan la salud y prevengan riesgos sanitarios.
Como órgano encargado de regular, controlar y vigilar los aspectos concernientes a la salud, corresponde a la Cofepris:
• El control y vigilancia de los establecimientos de salud.
• La prevención y el control de los efectos nocivos de los factores ambientales en la salud del hombre.
• La salud ocupacional y el saneamiento básico.
• El control sanitario de productos, servicios y de su importación y exportación y de los establecimientos dedicados al proceso de los productos.
• El control sanitario del proceso, uso, mantenimiento, importación, exportación y disposición final de equipos médicos, prótesis, órtesis, ayudas funcionales, agentes de diagnóstico, insumos de uso odontológico, materiales quirúrgicos, de curación y productos higiénicos, y de los establecimientos dedicados al proceso de los productos.
El control sanitario de la publicidad de las actividades, productos y servicios.
• El control sanitario de la disposición de órganos, tejidos y sus componentes, células de seres humanos.
• La sanidad internacional.
• El control sanitario de las donaciones y trasplantes de órganos, tejidos células de seres humanos.
• Evaluar los riesgos para la salud humana que generen los sitios en donde se manejen residuos peligrosos.
• Evaluar, expedir o revocar las autorizaciones que en las materias de su competencia se requieran.
• Imponer sanciones y aplicar medidas de seguridad.
• El control sanitario sobre la disposición de sangre.
Aún a pesar de ese amplio espectro de atribuciones, la actuación de la Cofepris se ha consolidado como una agencia de reconocimiento internacional al nivel de los más altos estándares regulatorios. No obstante, es necesario fortalecer sus capacidades técnicas, humanas y operativas, que le permitan atender la gran responsabilidad de garantizar la eficacia, la seguridad y la calidad de los bienes y servicios de consumo humano; entre los cuales destacan los medicamentos y los insumos para la salud.
El trabajo de la comisión es clave para que los ciudadanos tengan acceso oportuno a opciones que contribuyan a mejorar su salud, a disminuir la morbilidad y la mortalidad, a reducir el tiempo de hospitalizaciones y a mejorar su calidad de vida. Pero también tiene una importancia fundamental para apoyar el desarrollo económico de nuestro país pues los sectores industriales que regula producen poco más del 9.8 por ciento del PIB y regula 45 centavos de cada peso gastado por los hogares en México.
La Cofepris debe contar con esquemas sólidos de operación regulatoria para regular de manera efectiva y eficiente los productos e insumos que pudieran afectar la salud de las personas. Este órgano desconcentrado se encuentra ante retos importantes que requieren su consolidación como agencia la agencia reguladora de excelencia mediante la adopción de la tecnología y las mejores prácticas internacionales.
Debe promover una mayor transparencia y acceso ciudadano a la información; impulsar procesos ágiles de autorización, vigilancia y fomento sanitario basados en sistemas de calidad y mejora continua; promover el desarrollo económico y fomentar las mejores prácticas internacionales.
El propio programa de trabajo de la Cofepris 2018-2024, presenta siete acciones puntuales a desarrollar:
4.2. Fortalecer los mecanismos para normar y controlar las condiciones sanitarias tendientes a la reducción de riesgos a la salud para garantizar acciones y estrategias pertinentes de vigilancia y fomento sanitarios, promoción y prevención, con énfasis en la población en condición de vulnerabilidad.
4.2.1. Impulsar la adecuación de atribuciones de la Cofepris para optimizar sus funciones rectoras relativas al control de medicamentos, dispositivos médicos, bebidas y alimentos en todo el territorio nacional.
4.2.2. Designar personal profesional a los hospitales responsables de la implementación y seguimiento de acciones relacionadas con la farmacovigilancia.
4.2.3. Impulsar propuestas relacionadas con la simplificación de mecanismos para la autorización de apertura de establecimientos que brinden servicios de atención médica, evitando trámites burocráticos innecesarios y situaciones proclives a la corrupción.
4.2.4. Impulsar propuestas relacionadas con la eficacia de la Comisión de Control Analítico y Ampliación de Cobertura a fin de fortalecer la generación de resultados analíticos, resoluciones y dictámenes técnicos confiables y oportunos que favorezcan la protección de la salud de la población.
4.2.5. Coordinar la participación activa del sector salud, con diversos sectores para proponer, fortalecer o adecuar medidas regulatorias que propicien entornos saludables para la población.
4.2.6. Participar en el proceso interinstitucional relacionado con la regulación y legalización del cannabis, para anticipar adecuaciones que resulten procedentes en el sistema nacional de salud.
4.2.7. Promover la armonización de la normatividad en materia de investigación en salud para asegurar la protección de los derechos humanos de quienes participen en investigación, así como la distribución equitativa de los beneficios derivados de esta actividad.
Aunado a lo anterior, la reciente pandemia por Covid-19 nos ha mostrado, por un lado, serias debilidades de nuestro sistema regulatorio, pero también los poderosos resultados que se obtienen cuando las agencias regulatorias y sus entes regulados trabajan de manera coordinada en bienestar de la población.
Nuestro organismo regulador en materia sanitaria debe jugar un papel protagónico no sólo en materia de vigilancia y supervisión de toda una enorme gama de productos y servicios relacionados con la salud de la población, sino por el impacto que genera en materia económica. Las industrias que regula son aquellas que producen todo aquello que ingerimos, tomamos, nos untamos, nos aplicamos, inhalamos, es decir todo lo que entra de una u otra manera a nuestro organismo; por ello, una regulación eficaz y adecuada contribuye a que sea más competitiva.
Algunos aspectos que es necesario considerar para implementar acciones y programas para avanzar en el fortalecimiento de la regulación sanitaria son transparentar y homologar los criterios y estándares de decisión de los trámites y procedimientos de autorización sanitaria (principalmente registros sanitarios y modificaciones), con objeto de brindar certeza jurídica a los particulares. Es necesario, publicar los estándares técnico-científicos, así como los criterios de decisión para todos los trámites inscritos en el Registro Federal de Trámites y Servicios (RFTS) que aplica la Cofepris.
Se debe facilitar la trazabilidad y el seguimiento de los trámites en autorización por parte de la autoridad sanitaria y de los particulares, es necesario avanzar en la digitalización de los trámites de autorización sanitaria y, en particular, en aspectos y herramientas tales como la firma electrónica y carpetas o expedientes electrónicos.
La Cofepris debe avanzar en el fortalecimiento del sistema regulatorio como parte esencial de la política nacional de acceso a medicamentos y fomento al desarrollo y fabricación de productos médicos. Debe fortalecer sus planes de mejora continua para enfrentar demandas crecientes de tecnologías de salud más complejas. Fortalecer las especificidades regulatorias y su capacidad para regular cadenas de suministro globalizadas. Avanzar en el uso de evaluación comparativa de los sistemas regulatorios y sus implicaciones regionales y mundiales. Implementar prácticas que permitan mayor eficiencia y superación de brechas acorde al contexto específico que vive nuestro país, entre muchos otros.
Debe eficientar los mecanismos de vigilancia y las sanciones sobre la violación o incumplimiento de la regulación; apoyar el desarrollo de capacidades técnicas, humanas e institucionales en las entidades federativas así como de los diversos organismos a nivel regional y/o local, dedicados a la protección contra riesgos sanitarios; mejorar el intercambio de información y la coordinación institucional entre las diversas dependencias federales y entre los distintos ámbitos de gobierno con atribuciones en materia sanitaria.
Debe promover una cultura de protección contra riesgos sanitarios entre la población en general, incluyendo a la población infantil, y, especialmente, entre aquélla con mayor exposición y vulnerabilidad frente a riesgos específicos.
Establecer un sistema institucional de vigilancia activa con laboratorios para el control analítico de productos en puntos de entrada al país: fronteras, puertos y aeropuertos; e intensificar y dirigir las acciones de vigilancia focalizada en alimentos, tabaco, bebidas alcohólicas, medicamentos, bancos de sangre y hospitales, bajo criterios de riesgo sanitario sustentado en evidencia científica y establecer un sistema integral de respuesta pronta y eficaz a las alertas y emergencias sanitarias.
Fortalecer las instancias y mecanismos para verificar las prácticas de manufactura, manejo, comercialización y disposición de medicamentos, alimentos, productos y servicios, nacionales e importados, que presenten mayor potencial de riesgos sanitarios para la población.
Crear un grupo de verificadores especializados en el combate a prácticas ilegales que expongan a la población en materia de riesgos sanitarios, ligados a medicamentos, alimentos, bebidas, servicios y medio ambiente. Fortalecer su infraestructura física y tecnológica para eficientar procesos, entre otros.
Los retos son múltiples y es necesario avanzar en todos los frentes, pero para ello, es necesario que la Cofepris cuente con los recursos que se lo permitan; sin la disposición de recursos difícilmente avanzaremos en los retos y compromisos en esta materia.
Para ello es necesario que las autoridades que elaboran y aprueban el Presupuesto de Egresos de la Federación (SHCP y Cámara de Diputados) le destinen mayores recursos económicos.
Por la naturaleza de la función de la Comisión, el 90 por ciento de su presupuesto es para servicios personales (remuneraciones, seguridad social, estímulos y otras prestaciones sociales y económicas.
En los últimos años, se han dado cambios de titular y comisionados en la Cofepris, pero lamentablemente continúan los rezagos en la resolución de trámites y en sus procesos de control sanitario.
Con ello, hay retrasos en la autorización de nuevos medicamentos, se ha perdido el control sanitario de los alimentos importados, hay dudas en el desarrollo de biológicos como las vacuna “Abdalá” y “Patria” contra Covid-19 mientras la enfermedad sigue cobrando vidas, entre otros graves problemas para la salud de México.
De acuerdo con la Ley General de Salud a Cofepris le corresponde: Efectuar la evaluación de riesgos a la salud y definir la política de protección contra riesgos sanitarios, así como su instrumentación en establecimientos de salud; medicamentos y otros insumos para la salud; disposición de órganos y tejidos; alimentos y bebidas, productos cosméticos; tabaco, plaguicidas, sustancias tóxicas o peligrosas; suplementos alimenticios, así como de prevención y control de los efectos nocivos de los factores ambientales en la salud.
En conjunto estos sectores regulados por Cofepris representan 10 por ciento del PIB, así de grande es el terrible impacto que nos está generando su inoperancia.
Pese a su importancia estratégica para la salud de los mexicanos, dicha institución se encuentra en una parálisis peligrosa que nos está condenando al atraso, a la falta de innovación, a cancelaciones en inversión, a la carencia de nuevos medicamentos y tratamientos para muchas enfermedades y a perder nuestra capacidad de prevenir riesgos para la salud.
Tan grande es el rezago, que diversas empresas y organizaciones han iniciado recursos legales contra Cofepris para obtener autorizaciones, licencias o registros sanitarios.
A pesar de los anuncios de mejoras en procesos administrativos y de transparencia, y su paulatina implementación, como ha sido a través de los Acuerdos de equivalencia y sus modificaciones, la Plataforma de Trámites Autogestivos (DigiPRis), el Esquema de Celeridad para Abatir el Rezago (ECAR), la implementación de Trackerpris,1 así como la reciente Estrategia de Certidumbre Regulatoria para el Sector Farmacéutico,2 lo cierto es que no se tienen cifras específicas que permitan afirmar que se ha abatido el rezago.
La plataforma Trackerpris no refleja estatus de avance con respecto a su última actualización. Han repetido en varias ocasiones que se está trabajando en digitalizar los trámites que realiza la Cofepris, pero también sabemos que sigue habiendo trámites de 2018,2019, 2020 que todavía están por resolver.
En comunicados a la prensa, la Comisión ha señalado que “el aumento del 3 por ciento en la atención de lo ingresado, corresponde a un total de 5,720 trámites atendidos contra 5,537 que ingresaron”, 3 sin embargo, no se aclara qué tipo de trámites se resolvieron y no parece que se estén considerando los trámites históricamente rezagados.
Además, en septiembre de 2024, Cofepris ha reportado más de medio millón de trámites finalizados de manera 100 por ciento digital.4 Destacando que la nueva Plataforma Digital de Investigación y Ensayos Clínicos Digipris permite dejar atrás los trámites en papel y las citas presenciales, innovando en la forma de hacer regulación. Y que dicha plataforma hace posible realizar los trámites en un entorno digital, sin intermediarios, de manera directa y ágil.
Sin embargo, expertos han señalado que la complejidad del rezago se refleja en que, si bien se ha avanzado, aún es absolutamente insuficiente porque apenas se empieza a resolver el problema estructural y hacia adelante se deberá empezar a atacar el rezago histórico. En 2019 y 2020 Cofepris simplemente dejó sin atender más de la mitad (56 y 55 por ciento) de las solicitudes presentadas; para 2021 cuando llegó Alejandro Svarch a hacerse cargo, la falta de respuesta se redujo a 30 por ciento y para 2023 a 9 por ciento. De 10,748 que entraron en 2019, Cofepris respondió 4,774; para 2022 recibió 12,439 y respondió 11,323 trámites. Más de 1,000 quedaron sin responder.5
Por ello, la presente iniciativa propone precisar que los derechos provenientes por la prestación de servicios señalados en el capítulo XIV del título primer de las Ley Federal de Derecho se destinen a la Cofepris para el fortalecimiento de las actividades y servicios en materia de regulación, control, vigilancia y fomento sanitarios.
Dichos recursos le permitirán atender de forma eficaz y oportuna las atribuciones que tiene conferidas en la Ley General de Salud y demás normas aplicables; le permitirá alcanzar los mayores estándares de calidad regulatoria en beneficio de nuestra población.
De acuerdo con el artículo 2o. del Código Fiscal de la Federación las contribuciones para sufragar los gastos públicos se clasifican en impuestos, aportaciones de seguridad social, contribuciones de mejoras y derechos. Los derechos son las contribuciones establecidas en la Ley Federal de Derechos por recibir servicios que presta el Estado en sus funciones de derecho público, excepto cuando se presten por organismos descentralizados u órganos desconcentrados cuando, en este último caso, se trate de contraprestaciones que no se encuentren previstas en la Ley Federal de Derechos.
En el Título Primero, De los Derechos por la Prestación de Servicios, de la Ley Federal de Derechos, el Capítulo XIV, De la Secretaría de Salud, establece los derechos que se pagan por Autorizaciones en Materia Sanitaria y por el Fomento y Análisis Sanitario; el último artículo del capítulo, el artículo 195-L-4, establece que los ingresos que se obtengan por la recaudación de los derechos a que se refiere el presente Capítulo, se destinarán a la Secretaría de Salud, para el mantenimiento, conservación y operación de los servicios en materia de riesgo sanitario. No obstante, al no tener como destino específico a la Cofepris, terminan diseminados en toda la estructura de la Secretaría de Salud.
Por ello se propone modificar el artículo señalado, para establecer que, los ingresos que se obtengan por la recaudación de los derechos a que se refiere el presente Capítulo, se destinarán al órgano desconcentrado denominado Comisión Federal para la Protección contra Riesgos Sanitarios, para el fortalecimiento de las actividades y servicios en materia de regulación, control, vigilancia y fomento sanitarios.
Lo que permitirá asegurar la sustentabilidad financiera de la Cofepris al asegurar que la totalidad los ingresos provenientes por el pago de derechos en materia sanitaria le sean asignados a la Cofepris como parte de su presupuesto, al evitar que estos recursos tengan que entrar o mezclarse en la bolsa general de ingresos de la Tesorería de la Federación; que le permita la disponibilidad inmediata de los recursos, para fortalecer su capacidad para enfrentar los retos presentes y futuros.
De la misma forma, para fortalecer su autonomía, se contempla una modificación a la Ley General de Salud en los siguientes términos:
• La Comisión Federal para la Protección contra Riesgos Sanitarios, contará con independencia administrativa y financiera, y tendrá la capacidad de gestionar su presupuesto, recursos humanos y estructura organizativa.
• La Comisión Federal para la Protección contra Riesgos Sanitarios tomará sus decisiones basadas exclusivamente en evidencia científica, criterios técnicos y mejores prácticas internacionales en el campo de la regulación sanitaria.
• La Comisión Federal para la Protección contra Riesgos Sanitarios desarrollará y publicará procedimientos para la evaluación y aprobación de actividades, productos, servicios y establecimientos, asegurando que estos procesos sean transparentes y accesibles al público.
• La persona Comisionada Federal deberá acreditar al menos 8 años de experiencia en materia de regulación, control y fomento sanitario.
• Para el desarrollo de sus funciones, la Comisión Federal para la Protección contra Riesgos Sanitarios, contará con Comisionados de Autorización Sanitaria, de Operación Sanitaria, de Fomento Sanitario, de Evidencia y Manejo de Riesgos, de Control Analítico y Ampliación de Cobertura, cuyas atribuciones se detallarán en el reglamento interno, quienes serán designados por el Consejo de Salubridad General, a propuesta de la Persona Comisionada Federal. Los comisionados a los que se refiere el presente párrafo deberán contar con al menos 5 años de experiencia en la materia correspondiente a sus funciones.
• La Comisión Federal para la Protección contra Riesgos Sanitarios, contará con un órgano consultivo, denominado Consejo Consultivo de regulación y protección contra riesgos sanitarios, que se integrará con un cuerpo colegiado, integrado por expertos de los sectores privado, académico y social, que actuará como órgano de consulta en materias de regulación y protección contra riesgos sanitarios.
Comparativo de la propuesta de reforma legal:
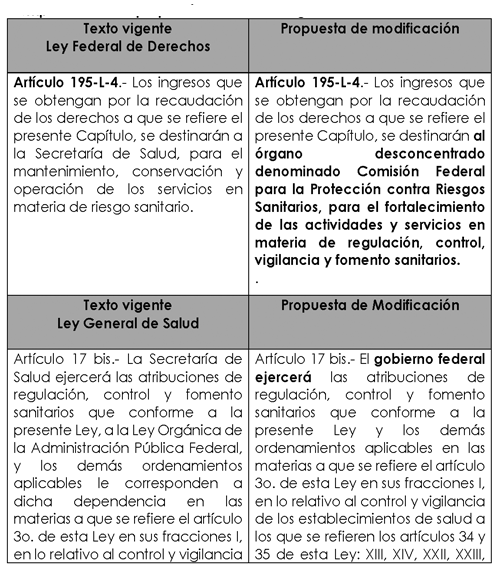




Por las razones expuestas, en ejercicio de la facultad que me confiere el artículo 71, fracción I, de la Constitución Política de los Estados Unidos Mexicanos, someto a consideración de esa soberanía la siguiente iniciativa con proyecto de
Decreto por el que se reforma la Ley Federal de Derechos y la Ley General de Salud, con el fin de fortalecer la autonomía, el financiamiento de la regulación, control, vigilancia y fomento sanitario que realiza Cofepris
Primero . Se reforma el artículo 195 L-4, de la Ley Federal de Derechos, para quedar como sigue:
Artículo 195-L-4 .- Los ingresos que se obtengan por la recaudación de los derechos a que se refiere el presente Capítulo, se destinarán al órgano desconcentrado denominado Comisión Federal para la Protección contra Riesgos Sanitarios, para el fortalecimiento de las actividades y servicios en materia de regulación, control, vigilancia y fomento sanitarios.
Segundo . Se reforma el primer párrafo y se adicionan un segundo, tercer y cuarto párrafos al artículo 17 Bis; se reforma el primer párrafo, la fracción I y el último párrafo del artículo 17 Bis 1; se reforma el primer párrafo y se adiciona un segundo y tercer párrafos al artículo 17 Bis 2, y se adiciona un a artículo 17 Bis 3, todos de la Ley General de Salud para quedar como sigue:
Artículo 17 bis.- El gobierno federal ejercerá las atribuciones de regulación, control y fomento sanitarios que conforme a la presente Ley y los demás ordenamientos aplicables en las materias a que se refiere el artículo 3o. de esta Ley en sus fracciones I, en lo relativo al control y vigilancia de los establecimientos de salud a los que se refieren los artículos 34 y 35 de esta Ley: XIII, XIV, XXII, XXIII, XXIV, XXV, XXVI, ésta salvo por lo que se refiere a cadáveres y XXVII, esta última salvo por lo que se refiere a personas, a través de un órgano descentralizado no sectorizado , que se denominará Comisión Federal para la Protección contra Riesgos Sanitarios.
La Comisión Federal para la Protección contra Riesgos Sanitarios, contará con independencia administrativa y financiera, y tendrá la capacidad de gestionar su presupuesto, recursos humanos y estructura organizativa.
La Comisión Federal para la Protección contra Riesgos Sanitarios tomará sus decisiones basadas exclusivamente en evidencia científica, criterios técnicos y mejores prácticas internacionales en el campo de la regulación sanitaria.
La Comisión Federal para la Protección contra Riesgos Sanitarios desarrollará y publicará procedimientos para la evaluación y aprobación de actividades, productos, servicios y establecimientos, asegurando que estos procesos sean transparentes y accesibles al público.
Artículo 17 bis 1.- El órgano descentralizado no sectorizado a que se refiere el artículo 17 bis, contará con independencia administrativa y financiera, y tendrá la capacidad de gestionar su presupuesto, recursos humanos y estructura organizativa. S u presupuesto estará constituido por:
I. Las asignaciones que establezca la Ley de Ingresos, la Ley de Derechos y el Presupuesto de Egresos de la Federación, y
II. Los recursos financieros que le sean asignados, así como aquellos que, en lo sucesivo, se destinen a su servicio.
Los ingresos que la Comisión Federal para la Protección contra Riesgos Sanitarios obtenga por concepto de donativos nacionales e internacionales, rescate de seguros y otros ingresos de carácter excepcional podrán ser recuperados por dicha Comisión y destinados a su gasto de operación, mismos que deberán ser etiquetados en el Presupuesto de Egresos de la Federación para el ejercicio fiscal correspondiente.
Artículo 17 bis 2.- Al frente de la Comisión Federal para la Protección contra Riesgos Sanitarios estará una persona Comisionada Federal, quien serán nombrada por el pleno del Consejo de Salubridad General para un periodo de 7 años, bajo el mecanismo que determine el Consejo.
La persona Comisionada Federal deberá acreditar al menos 8 años de experiencia en materia de regulación, control y fomento sanitario.
Para el desarrollo de sus funciones, la Comisión Federal para la Protección contra Riesgos Sanitarios, contará con Comisionados de Autorización Sanitaria, de Operación Sanitaria, de Fomento Sanitario, de Evidencia y Manejo de Riesgos, de Control Analítico y Ampliación de Cobertura, cuyas atribuciones se detallarán en el reglamento interno, quienes serán designados por el Consejo de Salubridad General, a propuesta de la Persona Comisionada Federal. Los comisionados a los que se refiere el presente párrafo deberán contar con al menos 5 años de experiencia en la materia correspondiente a sus funciones.
Artículo 17 bis 3- La Comisión Federal para la Protección contra Riesgos Sanitarios, contará con un órgano consultivo, denominado Consejo Consultivo de regulación y protección contra riesgos sanitarios, que se integrará con un cuerpo colegiado, integrado por expertos de los sectores privado, académico y social, que actuará como órgano de consulta en materias de regulación y protección contra riesgos sanitarios.
Este Consejo operará con total independencia y sus recomendaciones serán de carácter consultivo.
Los miembros serán seleccionados por el Consejo de Salubridad General, bajo criterios de experiencia, mérito y contribución relevante en sus campos de especialización. Los procedimientos de selección serán transparentes y públicos.
Transitorios
Primero. El presente Decreto entrará en vigor al día siguiente de su publicación en el Diario Oficial de la Federación.
Segundo. La Comisión Federal para la Protección contra Riesgos Sanitarios hará los ajustes necesarios a su reglamento interno y normatividad correspondiente para cumplir con el presente decreto en los 180 días posteriores su publicación en el Diario Oficial de la Federación.
Notas
1 https://trackerpris.cofepris.gob.mx/
2 https://www.gob.mx/cms/uploads/attachment/file/792036/Estrategia_de_Certidumbre_Regulatoria
_para_el_sector_Farmaceutico_enero_2023.pdf
3 https://www.eleconomista.com.mx/opinion/Insostenible-el-cuello-de-botel la-en-Cofepris-20220815-0010.html
4 https://www.gob.mx/cofepris/articulos/mas-de-medio-millon-de-tramites-f inalizados-de-manera-100-digital-en-cofepris
5 https://www.eleconomista.com.mx/opinion/La-complejidad-del-rezago-de-tr amites-en-Cofepris-20240723-0133.html
Dado en el Palacio Legislativo de San Lázaro, a 9 de octubre de 2024.
Diputado Éctor Jaime Ramírez Barba (rubrica)
Que reforma y adiciona diversas disposiciones de la Ley General de Salud, en materia de enfermedades raras, suscrita por el diputado Éctor Jaime Ramírez Barba y legisladores integrantes del Grupo Parlamentario del PAN
El que suscribe, Éctor Jaime Ramírez Barba y diputadas y diputados integrantes del Grupo Parlamentario del PAN, en la LXVI Legislatura de la Cámara de Diputados del honorable Congreso de la Unión, con fundamento en lo dispuesto en los artículos 71, fracción II, y 72 de la Constitución Política de los Estados Unidos Mexicanos; 6, numeral 1, 77 y 78 del Reglamento de la Cámara de Diputados, somete a consideración de esta soberanía la presente iniciativa con proyecto de decreto por el que se reforman y adicionan diversas disposiciones en la Ley General de Salud, en materia de enfermedades raras, al tenor de la siguiente
Exposición de Motivos
Las enfermedades raras, según la definición proporcionada por la Organización Mundial de la Salud (OMS), son aquellas condiciones médicas que afectan a una proporción reducida de la población, específicamente a menos de cinco personas por cada 10 mil habitantes.1 Este umbral establecido por la OMS refleja la baja prevalencia de estas enfermedades en comparación con otras condiciones de salud más comunes. Es importante destacar que, a pesar de su baja frecuencia, la suma total de enfermedades raras es considerable, superando las siete mil enfermedades identificadas hasta la fecha.
La rareza de estas enfermedades no solo se relaciona con su incidencia limitada en la población, sino también con la diversidad y complejidad de los trastornos que abarcan. Cada una de estas más de siete mil enfermedades raras presenta características únicas, lo que complica aún más su identificación, diagnóstico y tratamiento. Algunas de estas condiciones son genéticas, mientras que otras pueden ser adquiridas a lo largo de la vida, lo que añade una capa adicional de complejidad a su comprensión y manejo clínico.
El impacto de las enfermedades raras en la calidad de vida de los afectados es significativo. La falta de conocimiento sobre estas condiciones a menudo conduce a retrasos en el diagnóstico, lo que puede provocar la progresión no controlada de la enfermedad y la ausencia de tratamientos adecuados. Además, la naturaleza crónica y, en muchos casos, debilitante de estas enfermedades implica una necesidad continua de atención médica especializada y apoyo integral.
En ese sentido, la visión de los Objetivos de Desarrollo Sostenible es un mundo en el que nadie se quede atrás, incluidas las personas que padecen enfermedades raras. El hecho de que una enfermedad afecte a un número reducido de personas no la convierte en irrelevante o menos importante que las enfermedades que afectan a millones... director general de la OMS, doctor Tedros Adhanom Ghebreyesus, Declaración del Día de las Enfermedades Raras, febrero de 2018.2
La identificación de enfermedades raras representa un desafío significativo, ya que su baja prevalencia dificulta su reconocimiento y diagnóstico oportuno. Con frecuencia, los pacientes pasan por largos períodos sin un diagnóstico certero, lo que contribuye a la progresión de la enfermedad y a la falta de acceso a tratamientos adecuados. La falta de conciencia y conocimiento en el ámbito médico y la ausencia de herramientas de tamizaje ampliado contribuyen a este retraso en el diagnóstico.
La atención a pacientes con enfermedades raras requiere un enfoque integral y multidisciplinario. Es esencial proporcionar servicios de salud especializados que aborden las necesidades específicas de estos pacientes, incluyendo tratamientos personalizados, terapias de apoyo y seguimiento continuo. Además, se hace necesario fomentar la investigación y el desarrollo de medicamentos específicos para estas enfermedades, dada la escasez de opciones terapéuticas disponibles.
Los pacientes con enfermedades raras a menudo enfrentan dificultades para acceder a servicios de atención médica especializada y tratamientos adecuados. La atención integral debe considerar aspectos emocionales, sociales y económicos, garantizando la inclusión de los pacientes en la sociedad y proporcionando apoyo a sus familias. La creación de centros de referencia especializados y el acceso a terapias innovadoras son esenciales para satisfacer las necesidades específicas de esta población.
Los sistemas de salud enfrentan numerosos desafíos en la atención a pacientes con enfermedades raras. La falta de conocimiento y conciencia, la fragmentación en la atención médica, los altos costos de tratamientos específicos y la ausencia de registros nacionales que permitan una planificación adecuada son algunos de los obstáculos que impiden una respuesta eficaz a estas enfermedades. La coordinación a nivel nacional se vuelve fundamental para garantizar un abordaje coherente y efectivo.
En México se reconocían 20 enfermedades raras, como el Síndrome de Turner, Enfermedad de Pompe, Hemofilia, Espina Bífida, Fibrosis Quística, Histiocitosis, Hipotiroidismo Congénito, Fenilcetonuria, Galactosemia, Enfermedad de Gaucher Tipo 1, 2 y3, Enfermedad de Fabry, Hiperplasia Suprarrenal Congénita, Homocistinuria, entre otras.3 No obstante, de conformidad con el acuerdo por el que se reconocen las enfermedades raras incorporadas en la Clasificación Internacional de Enfermedades emitida por la Organización Mundial de la Salud, publicado por el Consejo de Salubridad General el 26 de junio de 2023, se reconocen en el país, las enfermedades raras incorporadas en la Clasificación Internacional de Enfermedades, emitida por la Organización Mundial de la Salud.
En ese sentido, dicho acuerdo establece medidas para:
Exhortar a las dependencias y entidades, tanto de la administración pública federales como local, que conforman el Sistema Nacional de Salud, a fortalecer la atención primaria a la salud, para proporcionar, en términos de las disposiciones jurídicas aplicables, el acceso a servicios de salud de calidad, accesibles, asequibles, seguros y oportunos, a las personas que viven con una enfermedad rara, con el objeto de cumplir con las finalidades del derecho a la protección de salud, establecidas en el artículo 2o de la Ley General de Salud.
Exhortar a las dependencias y entidades públicas, tanto federales como locales, del Sistema Nacional de Salud, a fortalecer los esquemas y mecanismos de información, análisis, estudio, investigación y capacitación de las enfermedades raras.
Que la Comisión del Compendio Nacional de Insumos para la Salud dará prioridad a la inclusión de medicamentos huérfanos, como tecnologías innovadoras que contribuyan a mejorar la calidad en la prestación de los servicios a la población.
Que las dependencias y entidades públicas, tanto federales como locales, del Sistema Nacional de Salud, en términos de lo ordenado en el artículo 29 de la Ley General de Salud, determinen de los insumos contenidos en el Compendio Nacional de Insumos para la Salud, la lista de medicamentos y otros insumos esenciales para la salud, para otorgar, en el ámbito de su competencia, la prestación de servicios de salud a la población.
Uno de los mayores retos en México es la falta de un marco regulatorio robusto que facilite el desarrollo y la aprobación de medicamentos para enfermedades raras. A diferencia de Estados Unidos y la Unión Europea, donde existen leyes y recomendaciones específicas para incentivar la investigación y el acceso a tratamientos, en México aún se carece de políticas integrales que aborden estas necesidades. Esta ausencia contribuye a la escasa disponibilidad de medicamentos y tratamientos especializados, aumentando las desigualdades en el acceso a la salud.
Además, las disparidades económicas y sociales en el país significan que muchas familias no tienen los recursos necesarios para costear tratamientos importados o asistir a centros médicos especializados, limitando aún más las oportunidades de mejorar la calidad de vida de los pacientes.
Los informes recientes de organismos como la Administración de Alimentos y Medicamentos de Estados Unidos (FDA) y la Agencia Europea de Medicamentos (EMA) ofrecen valiosas lecciones sobre cómo abordar estos desafíos. Entre las recomendaciones clave se destacan:
A. Fortalecimiento de mecanismos para integrar la opinión de los pacientes: Involucrar a las personas afectadas por enfermedades raras en todo el proceso de desarrollo de medicamentos puede garantizar que las soluciones propuestas realmente respondan a sus necesidades.
B. Fomento de la colaboración internacional: La cooperación entre agencias regulatorias permite compartir información y recursos, optimizando el proceso de aprobación y asegurando la calidad de los tratamientos disponibles.
C. Incentivos para la investigación y el desarrollo: Establecer beneficios fiscales y financieros para las empresas que inviertan en medicamentos para enfermedades raras puede acelerar la llegada de tratamientos al mercado.
D. Implementar estrategias similares en México podría transformar el panorama actual, facilitando el acceso a tratamientos innovadores y mejorando significativamente la calidad de vida de los pacientes.
La recopilación y el análisis de datos sobre la naturalidad de las enfermedades raras son esenciales para entender su impacto y diseñar intervenciones efectivas. Programas que apoyen la creación de registros de pacientes y estudios longitudinales pueden proporcionar una base sólida para la investigación científica y el desarrollo de tratamientos específicos. En México, es fundamental invertir en infraestructura y formación que permita la estandarización y el acceso a estos datos, facilitando así la colaboración entre instituciones y acelerando el proceso de descubrimiento y aprobación de nuevos medicamentos.
Es vital asegurar que todos los pacientes, independientemente de su ubicación geográfica o condición socioeconómica, tengan acceso equitativo a los tratamientos disponibles. Programas de apoyo financiero, cobertura médica ampliada y acceso a centros especializados son pasos necesarios para reducir las desigualdades existentes. Además, brindar apoyo psicológico y social a las familias impactadas puede aliviar el estrés y mejorar la cohesión comunitaria, creando un entorno más comprensivo y solidario.
El gobierno mexicano, en colaboración con instituciones privadas y organizaciones no gubernamentales, debe priorizar la formulación e implementación de políticas que aborden las necesidades de las personas con enfermedades raras. Inspirarse en las recomendaciones de organismos internacionales y adaptarlas al contexto local es un camino viable para avanzar hacia un sistema de salud más inclusivo y eficiente.
Además, es crucial fomentar la conciencia pública sobre estas condiciones, eliminando estigmas y promoviendo una cultura de empatía y apoyo. Las historias de lucha y resiliencia de quienes viven con enfermedades raras pueden servir como poderosos testimonios para movilizar recursos y generar un cambio significativo en la percepción social y las políticas de salud.
Aunque el camino por recorrer es largo, existen oportunidades para transformar la realidad de las enfermedades raras en México. La implementación de estrategias regulatorias flexibles, la promoción de la investigación colaborativa y el fortalecimiento del apoyo a pacientes y familias son pilares fundamentales para lograr un avance sostenible.
Es responsabilidad de todos —gobierno, sector privado, comunidad científica y sociedad en general— unir esfuerzos para garantizar que nadie quede atrás en la lucha contra las enfermedades raras. Solo a través de un compromiso colectivo y una acción decidida podremos construir un futuro donde cada persona, independientemente de su condición, tenga acceso a la atención y los recursos necesarios para llevar una vida plena y digna.
La empatía y la solidaridad deben guiar nuestras acciones, reconociendo que detrás de cada diagnóstico existe una historia única y valiente. Al enfrentar juntos estos desafíos, podemos cerrar las brechas existentes y ofrecer esperanza a quienes más lo necesitan.
Reconocer la existencia de las enfermedades raras no solo arroja luz sobre la experiencia de quienes las padecen, sino que también marca un hito crucial en la promoción de la investigación y el acceso a la atención médica.
La visibilidad de estas enfermedades impulsa una mayor conciencia pública, reduciendo el estigma y fomentando un entendimiento más profundo de las complejidades asociadas con estos trastornos poco comunes. Al hacerlo, se establece una base sólida para la promoción de la investigación científica en el campo de las enfermedades raras, abriendo la puerta a nuevos descubrimientos y tratamientos innovadores.
La visibilidad también desempeña un papel esencial en facilitar el diagnóstico temprano de las enfermedades raras. Con una mayor conciencia, los profesionales de la salud pueden estar mejor preparados para reconocer los síntomas, lo que lleva a diagnósticos más rápidos y precisos.
En ese contexto, en principio, las instituciones de salud deben impulsar acciones para la detección oportuna y tratamiento de las enfermedades raras a través de la ampliación del tamiz neonatal, el desarrollo de pruebas diagnósticas e investigación.
La ampliación del tamiz neonatal constituye una medida crucial para la detección temprana de enfermedades raras. La inclusión de pruebas específicas en el tamiz neonatal permitirá identificar posibles trastornos desde las primeras etapas de la vida, facilitando un diagnóstico oportuno y el inicio de intervenciones terapéuticas antes de que se desarrollen complicaciones severas. Este enfoque preventivo es esencial para mejorar los resultados de salud a largo plazo de los niños afectados.
A su vez, la investigación terapéutica representa una faceta esencial en la mejora de la atención a pacientes con enfermedades raras. El impulso a la investigación no solo busca comprender mejor la base genética y molecular de estas enfermedades, sino también desarrollar tratamientos específicos y personalizados. La promoción de estudios clínicos y la colaboración con la comunidad científica nacional e internacional son elementos clave para avanzar en el conocimiento y abordaje de estas condiciones, ofreciendo esperanza a aquellos afectados y sus familias.
Quienes firmamos esta iniciativa consideramos que, la identificación y abordaje de las enfermedades raras demandan un enfoque más específico y personalizado en la atención médica.
Ante la necesidad de mejorar la detección temprana, el diagnóstico oportuno y la atención integral a los pacientes con enfermedades raras, proponemos la modificación de la Ley General de Salud para establecer un marco legal que fortalezca las acciones en este ámbito.
La propuesta de reforma a la Ley General de Salud representa un paso significativo hacia la mejora de la atención a pacientes con enfermedades raras en el contexto de la salud pública. La modificación se centra en tres áreas cruciales: la detección temprana, el diagnóstico oportuno y la coordinación a nivel nacional. En primer lugar, la ampliación del tamiz neonatal con pruebas específicas para enfermedades raras busca identificar a los pacientes afectados en las etapas iniciales de la vida, permitiendo así intervenciones tempranas que pueden mejorar significativamente los resultados de salud.
La creación de un registro nacional de enfermedades raras es otro componente clave de la reforma. Este registro proporcionará una base de datos centralizada y actualizada sobre la prevalencia, características y tratamientos de las diversas enfermedades raras en el país. Esta información será invaluable para la planificación estratégica, asignación de recursos y desarrollo de políticas de salud adaptadas a las necesidades específicas de los pacientes con enfermedades raras.
La instauración de la Comisión Nacional de Enfermedades Raras destaca el compromiso de coordinación a nivel gubernamental para abordar estos desafíos de manera integral. La colaboración entre expertos, profesionales de la salud, investigadores y organizaciones de pacientes, bajo el liderazgo de esta comisión, permitirá una gestión más efectiva de los recursos y una respuesta más coordinada a las complejidades asociadas con las enfermedades raras. En conjunto, estas reformas no solo fortalecerán el sistema de salud para enfrentar las enfermedades raras, sino que también mejorarán la calidad de vida de aquellos afectados y sus familias.
Cada pequeña victoria en la lucha contra una enfermedad rara es un gran paso hacia la esperanza.
Artículo Único. Se reforman el segundo párrafo y la fracción II del artículo 61; y se adicionan el capítulo IV, “Enfermedades Raras”, adicionándose los artículos 161 Bis 1, 161 Bis 2, 161 Bis 3, 161 Bis 4, 161 Bis 5, 161 Bis 6 y 161 Bis 1, todos en la Ley General de Salud, para quedar como sigue:
Artículo 61.- ...
La atención materno-infantil tiene carácter prioritario, garantizando su desarrollo integral y el disfrute pleno y efectivo a la protección y el disfrute del más alto nivel posible de salud, en atención al interés superior de la niñez , y comprende, entre otras, las siguientes acciones:
I. ...
I Bis. ...
II. La atención del niño y la vigilancia de su crecimiento, desarrollo integral, incluyendo la promoción de la vacunación oportuna, atención prenatal, así como la prevención y detección de las condiciones y enfermedades hereditarias, congénitas, así como aquellas consideradas enfermedades raras, y en su caso atención, que incluya la aplicación de pruebas del tamizaje ampliado, tamiz metabólico ampliado , y su salud visual, garantizando la atención integral, el acceso a los tratamientos e intervenciones médicas necesarias y, en su caso, asesoramiento genético.
Capítulo IV
Enfermedades Raras
Artículo 161 Bis 1. Las enfermedades raras son aquellas que se presentan en menos de cinco personas por cada 10 mil habitantes y existen más de siete mil enfermedades.
Se reconocen en el país, las enfermedades raras incorporadas en la Clasificación Internacional de Enfermedades, emitida por la Organización Mundial de la Salud.
Las dependencias y entidades, tanto de la administración pública federales como local, que conforman el Sistema Nacional de Salud, deberán fortalecer la atención primaria a la salud, para proporcionar, en términos de las disposiciones jurídicas aplicables, el acceso a servicios de salud de calidad, accesibles, asequibles, seguros y oportunos, a las personas que viven con una enfermedad rara.
Artículo 161 Bis 2. Es obligación de la Secretaría de Salud y sus homólogas en las entidades federativas, fortalecer los esquemas y mecanismos de información, análisis, estudio, investigación y capacitación de las enfermedades raras.
Artículo 161 BIS 3. La Comisión del Compendio Nacional de Insumos para la Salud dará prioridad a la inclusión de medicamentos huérfanos, como tecnologías innovadoras que contribuyan a mejorar la calidad en la prestación de los servicios a la población.
Artículo 161 Bis 4. La Comisión Nacional de Enfermedades Raras es un órgano desconcentrado, adscrito a la Secretaría de Salud, con la finalidad de coordinar y promover acciones específicas para la atención integral de las enfermedades raras en el territorio nacional.
Artículo 161 Bis 5. La Comisión Nacional de Enfermedades Raras estará integrada por un equipo multidisciplinario de expertos en áreas relevantes, incluyendo genética, pediatría, neurología, oncología, epidemiología, representantes de asociaciones de pacientes con enfermedades raras. La composición deberá reflejar la diversidad de las enfermedades raras y las necesidades de los pacientes.
Artículo 161 Bis 6. La Comisión Nacional de Enfermedades Raras tendrá las siguientes atribuciones:
I. Coordinar acciones a nivel nacional para la detección temprana, diagnóstico oportuno y atención integral de las enfermedades raras;
II. Proponer y desarrollar políticas, estrategias y planes de acción para mejorar la atención de las enfermedades raras, considerando la diversidad de estas condiciones y las necesidades específicas de los pacientes;
III. Supervisar y gestionar el Registro Nacional de Enfermedades Raras, asegurando la calidad, confidencialidad y accesibilidad de la información;
IV. Fomentar la investigación científica y el desarrollo de tratamientos específicos para enfermedades raras, promoviendo la colaboración con instituciones de investigación y la participación de la comunidad científica;
V. Establecer y fortalecer vínculos de colaboración con organizaciones internacionales, instituciones de salud de otros países y redes especializadas en enfermedades raras;
VI. Implementar programas de educación y concientización dirigidos a profesionales de la salud, pacientes, familiares y la sociedad en general, para mejorar la comprensión y el manejo de las enfermedades raras;
VII. Desarrollar programas de apoyo emocional, social y económico para pacientes y sus familias, considerando las cargas asociadas con las enfermedades raras;
VIII. Fomentar la aplicación de pruebas de tamiz ampliado para el diagnóstico oportuno de las enfermedades raras;
IX. Implementar programas educativos dirigidos a profesionales de la salud, laboratorios clínicos y otros actores relevantes, destacando la importancia de la detección temprana mediante pruebas de tamiz ampliado;
X. Identificar las necesidades específicas de tratamientos para enfermedades raras, considerando la diversidad de estas condiciones y las particularidades genéticas que puedan influir en la respuesta a los tratamientos;
XI. incentivar la investigación y desarrollo de medicamentos huérfanos para enfermedades raras;
XII. Colaborar con las autoridades regulatorias para facilitar y agilizar los procesos de aprobación y registro de medicamentos huérfanos;
XIII. Establecer colaboraciones con la industria farmacéutica y otras entidades relevantes para incentivar la investigación y desarrollo de medicamentos huérfanos para enfermedades raras;
XIV. Fomentar procesos regulatorios a estándares internacionales reconocidos para medicamentos huérfanos, asegurando la alineación con mejores prácticas, y
XV. Las que se determinen en su reglamento interior.
Artículo 161 Bis 7. El Registro Nacional de Enfermedades Raras tendrá una base poblacional, se integrará de la información proveniente del Sistema Nacional de Información Básica en Materia de Salud y contará con la siguiente información:
I. Clasificación de cada enfermedad rara, identificando su naturaleza genética, metabólica, neurológica, entre otras categorías;
II. Descripción de las características clínicas y síntomas asociados con cada enfermedad;
III. Historial ocupacional y laboral, relevante para comprender posibles exposiciones ambientales o laborales que puedan estar vinculadas a la enfermedad rara;
IV. Protocolos y criterios de diagnóstico para cada enfermedad rara;
V. Fecha de diagnóstico;
VI. Información sobre las pruebas y técnicas utilizadas para la detección temprana y confirmación del diagnóstico;
VII. Registro de tratamientos existentes y terapias recomendadas para cada enfermedad rara;
VIII. Información sobre la disponibilidad y accesibilidad de medicamentos y terapias especializadas;
IX. Seguimiento de la eficacia de tratamientos y resultados a largo plazo;
X. Descripción de la incidencia y el estado de la enfermedad;
XI. Estadísticas demográficas relacionadas con la prevalencia de cada enfermedad rara;
XII. Geolocalización detallada para analizar dispersiones geográficas y posibles agrupaciones comunitarias de enfermedades raras;
XIII. Evaluación de la dispersión geográfica de los casos, identificando posibles patrones geográficos de concentración;
XIV. Datos para identificar posibles predisposiciones genéticas en comunidades específicas;
XV. Desglose de la base poblacional afectada por cada enfermedad, incluyendo edad, género, y cualquier otra característica relevante, y
XVI. Información sobre la calidad de vida de los pacientes y su participación en la sociedad.
Transitorios
Primero. El presente decreto entrará en vigor el día siguiente al de su publicación en el Diario Oficial de la Federación.
Segundo.- El Ejecutivo federal, a través de las Secretarías de Salud, y de Hacienda y Crédito Público, establecerán las previsiones presupuestales, de manera progresiva y con cargo a los techos presupuestales autorizados, que permitan la implementación de las pruebas del Tamiz Metabólico Ampliado en el sistema público de salud y el acceso a los tratamientos, intervenciones médicas necesarias y, en su caso, asesoramiento genético a los padres o tutores.
Segundo.- El Ejecutivo federal, a través de las Secretarías de Salud y de Hacienda y Crédito Público, establecerán las previsiones presupuestales, de manera progresiva y con cargo a los techos presupuestales autorizados, que permitan la implementación del Registro Nacional de Enfermedades Raras.
Tercero.- El Ejecutivo federal, a través de las Secretaría de Salud, emitirá el Reglamento Interior de la Comisión Nacional de Enfermedades Raras, para su funcionamiento, en un plazo de 180 días contados a la entrada en vigor del presente decreto.
Cuarto.- La Secretaría de Salud realizará las adecuaciones pertinentes a las normas oficiales mexicanas en la materia, para dar cumplimiento a lo establecido en el presente decreto, en el plazo máximo de 180 días naturales a su entrada en vigor.
Notas
1 Organización Mundial de la Salud (OMS). https://www.who.int/news-room/detail/27-02-2018-statement-for-rare-dise ase-day
2 Rare diseases international. https://www.rarediseasesinternational.org/es/working-with-the-who/
3 Secretaría de Salud del gobierno federal. https://www.gob.mx/salud/articulos/que-son-las-enfermedades-raras-19328 0#:~:text=De%20acuerdo%20con%20la%20Organizaci%C3%B3n,m%C3%A1s%20de%20s iete%20mil%20enfermedades.
Dado en el Palacio Legislativo de San Lázaro, a 9 de octubre de 2024.
Diputado Éctor Jaime Ramírez Barba (rubrica)