Gaceta Parlamentaria, año XVI, número 3865-I, jueves 19 de septiembre de 2013
- De la Secretaría de Gobernación, con la que remite contestación a punto de acuerdo, aprobado por la Cámara de Diputados, relativo a la cancelación del registro de Endosulfán en México, en cumplimiento del Convenio de Estocolmo
- De la Secretaría de Gobernación, con la que remite contestación a punto de acuerdo, aprobado por la Comisión Permanente correspondiente al primer receso, a fin de que se evalúen los permisos de empresas transnacionales para sembrar maíz transgénico
Solicitudes de licencia
De la Secretaría de Gobernación, con la que remite contestación a punto de acuerdo, aprobado por la Cámara de Diputados, relativo a la cancelación del registro de Endosulfán en México, en cumplimiento del Convenio de Estocolmo
Secretarios de la Cámara de Diputados del Honorable Congreso de la Unión
Presentes
En respuesta al oficio número D.G.P.L. 62-II-7-681 signado por, la diputada Patricia Elena Retamoza Vega, vicepresidenta de la Mesa Directiva de ese órgano legislativo, me permito remitir para los fines procedentes, copia del similar número 170/UOIPS/DGAVS/790/2013 suscrito por la licenciada Pilar Torre Canales, directora general adjunta de Vinculación Social de la Secretaría de Salud, así como del anexo que en él se menciona, mediante los cuales responde el punto de acuerdo relativo a cancelar los permisos de importación de endosulfán en México, y se inicie el procedimiento administrativo para la cancelación definitiva de las autorizaciones de uso otorgadas, así como reportar los avances en la implementación de la decisión SC-5-4.
Sin otro particular, aprovecho la ocasión para reiterarles la seguridad de mi consideración distinguida.
Licenciado Valentín Martínez Garza (rúbrica)
Director General Adjunto de Proceso Legislativo
Por ausencia del titular de la Unidad de Enlace Legislativo, con fundamento en lo dispuesto por el artículo 132 del Reglamento Interior de la Secretaría de Gobernación
Unidad de Enlace Legislativo de la Secretaría de Gobernación
Presente
Me refiero al oficio SEL/UEL/311/690/13, mediante el cual se informa del punto de acuerdo aprobado por el pleno de la Cámara de Diputados del honorable Congreso de la Unión, en sesión celebrada el lunes 29 de abril de 2013, que a continuación se transcribe:
Primero. La Cámara de Diputados del honorable Congreso de la Unión exhorta respetuosamente a la titular de la Secretaría de Salud para que por medio de la Comisión Federal para la Protección contra Riesgos Sanitarios, a corto plazo, cancele los permisos de importación de endosulfán en México, y se inicie el procedimiento administrativo para la cancelación definitiva de las autorizaciones de uso otorgadas, antes de la sexta Conferencia de las Partes del Convenio de Estocolmo a celebrarse del domingo 28 de abril al sábado 11 de mayo del 2013, con el fin de reportar los avances en la implantación de la decisión SC-54, y lograr así una mejor protección a la salud de la población y el medio ambiente en nuestro país.
Segundo. La Cámara de Diputados del honorable Congreso de la Unión exhorta respetuosamente al titular de la Secretaría de Agricultura, Ganadería, Desarrollo Rural, Pesca y Alimentación, a que desarrolle y aplique un programa para la difusión e implementación de alternativas al endosulfán que incluya opciones no químicas, considerando la decisión SC-54: Programa de trabajo sobre endosulfán, con las recomendaciones e informes del Comité de Revisión de COP y las experiencias de expertos y organizaciones de productores en manejo agroecológico de plagas, agricultura orgánica; así como la coordinación y participación de universidades, centros de investigación, empresas que ofrecen insumos no químico-sintéticos para el control de plagas, y grupos ciudadanos y ambientalistas, con el fin de que, se establezcan apoyos para una mayor difusión y capacitación sobre estas altemativas a las organizaciones de productores en el país.
Al respecto, por instrucciones del licenciado Rodrigo Reina Liceaga, titular de la Unidad Coordinadora de Vinculación y Participación Social, me permito acompañar oficio número 467 suscrito por el licenciado Leonardo Menes Salís, coordinador general Jurídico y Consultivo de la Comisión Federal de Protección contra Riesgos Sanitarios.
Con base en lo anterior, he de agradecer su amable intervención a efecto de remitir esta información al órgano legislativo para su desahogo.
Sin otro particular, aprovecho la ocasión para enviarle un cordial saludo.
Atentamente
Licenciada Pilar Torre Canales (rúbrica)
Directora General Adjunta de Vinculación Social
Licenciada Pilar Torre Canales
Directora General Adjunta de Vinculación Social de la Secretaría de Salud
Presente
Con fundamento en los artículos 4o., párrafo cuarto, 8 y 90 de la Constitución Política de los Estados Unidos Mexicanos; 17 Bis de la Ley General de Salud; 2o. inciso c), fracción X, del Reglamento Interior de la Secretaría de Salud; 18, fracción II y XVI del Reglamento de la Comisión Federal para la Protección contra Riesgos Sanitarios y en atención a su oficio número 170/UCVPS/DGAVS/430/2013 a través del cual el remite el punto de acuerdo aprobado el 29 de abril del presente año en la Cámara de Diputados del honorable Congreso de la Unión consistente en el exhorto a la titular de la Secretaría de Salud para que por medio de la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris o Comisión Federal) cancele en el corto plazo los permisos de importación de edusulfán en México, y se inicie un procedimiento administrativo para la cancelación definitiva de las autorizaciones de uso otorgadas antes de la sexta Conferencia de las Partes del Convenio de Estocolmo a celebrarse del 28 de abril al 11 de mayo de 2013, con el fin de reportar los avances en la implementación de la desición SC-54, y lograr así una mejor protección a la salud de la población y el medio ambiente en nuestro país, le comento lo siguiente.
En aras de dar cumplimiento al Convenio de Estocolmo, firmado por el gobierno mexicano el 22 de mayo de 2001, esta Comisión Federal para la Protección contra Riesgos Sanitarios ha realizado las siguientes acciones:
El 8 de mayo de 2013, se realizó una reunión de trabajo con la Unión Mexicana de Fabricantes y Formuladores de Agroquímicos, AC, y la Asociación Mexicana de la Industria Fitosanitaria, AC, en la cual se alcanzaron los siguientes acuerdos:
1. A partir del 1 de enero de 2013 ya no hay autorizaciones de importación de endosulfán.
2. Quedan cancelados todos los permisos de importación de endosulfán, a partir del i de enero de 2013.
3. La Cofepris permitirá agotar los inventarios existentes de endosulfán, para lo cual señala como fecha lúimite el 31 de diciembre de 2014.
4. La industria realizará todas las gestiones necesarias a fin de reportar a la Cofepris cada seis meses los movimientos de sus inventarios.
5. Una vez que se agoten los inventarios a que hace referencia el numeral 3 o bien fenezca el término otorgado para ello (31 de diciembre de 2014), los titulares de los registros sanitarios relacionados con endosulfán solicitarán a la Cofepris a partir del 1 de enero de 2015 iniciará los correspondientes procedimientos de revocación respecto de los registros sanitarios en comento.
De igual manera, esta comisión federal cuenta con evidencia de que el periodo comprendido de febrero de 2011 a diciembre de 2012, se emitieron 14 permisos de importación, de los cuales únicamente cinco se encontraban vigentes hasta el 26 de abril de 2013, siendo los siguientes:
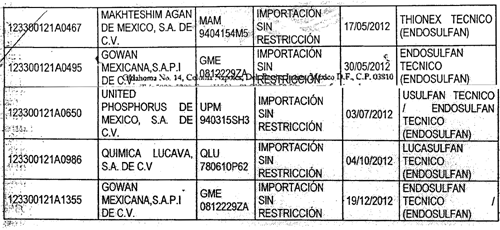
En tal virtud y cumplimiento de los acuerdos alcanzados en la reunión celebrada el 8 de mayo de 2013, la Cofepris canceló los siguientes permisos de importación:
• Permiso de importación número 123300121A0467, otorgado a Makhteshim Agan de México, SA de CV, para el producto Thionex Técnico (endusolfán), cancelado mediante oficio 133300EL780316, de 27 de mayo de 2013, que fue notificado personalmente a la empresa en cita con fecha 29 de mayo de 2013.
• Permiso de importación número 123300121A0650, otorgado a United Phosphorus de México, SA de CV, para el producto denominado Usulfán Técnico (endusolfán), cancelado mediante oficio 133300EL780316, de 27 de mayo de 2013, y notificado personalmente a la empresa en cita el 18 de junio de 2013.
• Permiso de importación número 123300121A0986, otorgado a Química Lucava, SA de CV, para el producto denominado Lucasulfán Técnico (endusolfán), cancelado mediante oficio 133300EL780354 de 10 de junio de 2013, y notificado personalmente a la empresa en cita el 18 de junio de 2013.
Cabe señalar que en relación con el permiso sanitario de importación número 123300121A0495, otorgado a Gowan Mexicana, SAPI de CV, la vigencia de éste feneció el pasado 30 de mayo de 2013.
Finalmente le comunico que Cofepris tiene conocimiento de la existencia de 84 registros sanitarios respecto de los cuales al día de hoy se ha solicitado a esta comisión federal la revocación voluntaria de 9 de ellos.
Sin otro particular, le envío un saludo.
Sufragio Efectivo. No Reelección.
Leonardo Menes Solís (rúbrica)
Coordinador General Jurídico y Consultivo
De la Secretaría de Gobernación, con la que remite contestación a punto de acuerdo, aprobado por la Comisión Permanente correspondiente al primer receso, a fin de que se evalúen los permisos de empresas transnacionales para sembrar maíz transgénico
México, DF, a 13 de septiembre de 2013.
Secretarios de la Cámara de Diputados del Honorable Congreso de la Unión
Presentes
En respuesta al oficio número DGPL 62-II-8-0794, signado por el diputado Francisco Arroyo Vieyra, presidente de la Mesa Directiva de la Comisión Permanente del honorable Congreso de la Unión, me permito remitir, para los fines procedentes, copia del similar número 112.2.668/2013, suscrito por el licenciado Francisco Olvera Acevedo, director general adjunto de Estudios Interinstitucionales de la Secretaría de Agricultura, Ganadería, Desarrollo Rural, Pesca y Alimentación, así como del anexo que en el mismo se menciona, mediante los cuales responde el punto de acuerdo relativo a realizar una evaluación de los permisos que se han otorgado para la siembra de maíz transgénico en nuestro país a las empresas trasnacionales Monsanto, Pionner y Dow Agroscience.
Sin otro particular, aprovecho la ocasión para reiterarles la seguridad de mi consideración distinguida.
Licenciado Valentín Martínez Garza (rúbrica)
Director General Adjunto de Proceso Legislativo
Por ausencia del titular de la Unidad de Enlace Legislativo, con fundamento en lo dispuesto por el artículo 132 del Reglamento Interior de la Secretaría de Gobernación.
Licenciado Valentín Martínez Garza
Director General Adjunto de Proceso Legislativo de la Secretaría de Gobernación
Presente
México, DF, a 2 de septiembre de 2013.
En atención a su oficio número SEL/UEL/31/0082/13, del 16 de enero de 2013, por el que nos remite punto de acuerdo aprobado por el honorable Congreso de la unión durante la sesión ordinaria del 166 de enero de 2013, mediante el cual se exhorta al titular de la Secretaría de Agricultura, Ganadería, Desarrollo Rural, Pesca y Alimentación, y al titular de la Secretaría de medio Ambiente y Recursos Naturales para que realice una evaluación de los permisos que se han otorgado para la siembra de maíz transgénico en nuestro país a las empresas trasnacionales Monsanto, Pionner y Dow Agroscience y, en su caso, revocar, negar y evitar aquellos que atenten contra la tierra, la producción y la salud de los mexicanos, de acuerdo a lo establecido en el artículo 69 de la Ley de Bioseguridad de Organismos Genéticamente Modificados; implementen medidas e incentivos a fin de promover estrategias que protejan la diversidad del maíz y preserven las semillas nativas, evitando con ello que se vuelvan dependientes de las transgénica y, en consecuencia, reducir los riesgos de contaminación que traen consigo para las cosechas, lo cual ha sido constatado por numerosos estudios de nivel mundial, me permito hacerle llegar la siguiente documentación:
Sobre el particular, adjuntamos a la presente información las observaciones y comentarios que sobre el tema nos hizo llegar el Servicio nacional de Sanidad, Inocuidad y Calidad Agropecuaria, mediante oficio número BOO.050205463 del 29 de agosto de 2013, con el cual se da respuesta a la información requerida.
Sin más por el momento, le reitero las seguridades de mi distinguida consideración.
Atentamente
Licenciado Francisco Olvera Acevedo (rúbrica)
Director General Adjunto de Estudios Interinstitucionales
Volante Senasica. 00072/2013
Registro folio DGJ.- 00415/2013
Número de oficio B00. 05.02- 05463
México, DF, a 29 de agosto de 2013
Ingeniero Héctor René García Quiñones
Coordinador General de Enlace Sectorial
Presente
Me refiero a su solicitud de comentarios relacionados con el punto de acuerdo aprobado de urgente y obvia resolución durante la sesión ordinaria del 16 de enero del presente año presentado por el diputado de la Revolución Democrática Luis Xariel Espinoza Cházaro, que contiene los siguientes resolutivos:
Primero . Realizar una evaluación de los permisos que se han otorgado para la siembra de maíz transgénico en nuestro país a las empresas trasnacionales Monsanto, Pioneer y Dow Agroscience y, en su caso, revocar, negar y evitar aquellos que atenten contra la tierra, la producción y la salud de los mexicanos, de acuerdo a lo establecido en el artículo 69 de la Ley de Bioseguridad de Organismos Genéticamente Modificados.
Segundo . Implementar medidas e incentivos a fin de promover estrategias que protejan la diversidad del maíz y preserven las semillas nativas, evitando con ello, que se vuelvan dependientes de las transgénicas y, en consecuencia, reducir los riesgos de contaminación que traen consigo para las cosechas, lo cual ha sido constatado por numerosos estudios a nivel mundial.
Sobre el particular, le comento que de conformidad con la consulta realizada al área técnica y operativa con injerencia en el tema (Dirección General de Inocuidad Agroalimentaria, Acuícola y Pesquera), me permito señalar lo siguiente:
México, como otros países, firmo en el año 2000 el Protocolo de Cartagena sobre Seguridad de la Biotecnología del Convenio sobre la Diversidad Biológica, el cual es el instrumento más importante a nivel internacional en materia de protección de la diversidad biológica.
En este contexto, el 18 de marzo de 2005, se publicó en el Diario Oficial de la Federación la Ley de Bioseguridad de Organismos Genéticamente Modificados, con el objeto de regular las actividades de utilización confinada, liberación experiencial, liberación en programas piloto, liberación comercial, comercialización, importación y exportación de organismos genéticamente modificados, a fin de prevenir, evitar y reducir los posibles riesgos que esas actividades pudieran ocasionar a la salud humana o al medio ambiente y a la diversidad biológica o a la sanidad animal, vegetal y acuícola, confiriéndole a la Secretaria de Agricultura, Ganadería, Desarrollo Rural, Pesca y Alimentación, facultades y atribuciones directas, las cuales se establecieron de los artículos 12 y 13 respectivamente de la ley en comento.
A partir de dicha publicación se comenzó con la generación de diversos instrumentos normativos que fortalecieron el marco regulatorio, dando mayor certeza técnico-jurídica a la autoridad competente, para la emisión de permisos de liberación al ambiente de organismos genéticamente modificados. En este sentido, el 19 de marzo del 2008 se publicó el Reglamento de la Ley de Bioseguridad de Organismos Genéticamente Modificados, el cual fue modificado el 6 de marzo de 2009, incluyendo el Régimen de Protección Especial del Maíz, mismo que permite realizar las actividades de liberación de dicho cultivo, en etapa experimental.
Asimismo, el secretario del ramo, el 22 de junio de 2009 publicó el acuerdo por el que se delegan en el titular del Servicio Nacional de Sanidad, Inocuidad y Calidad Agroalimentaria y en los directores generales de Sanidad Vegetal, Salud Animal e Inocuidad Agroalimentaria, Acuícola y Pesquera las facultades y funciones que se indican, dando atribuciones a este Servicio Nacional de Sanidad Inocuidad y Calidad Agroalimentaria para resolver sobre las solicitudes y, en su caso la expedición de permisos de liberación al ambiente de organismos genéticamente modificados, con la finalidad de atender puntualmente los asuntos relacionados con dichos organismos en el ámbito de competencia de la Sagarpa sustentando la elaboración y emisión del dictamen técnico respectivo.
En ese orden de ideas, el 2 de noviembre de 2012 fue publicado en el Diario Oficial de la Federación el acuerdo por el que se determinan centros de origen y centro de diversidad genética del maíz, el cual en su anexo II establece los centros de diversidad genética del maíz y sus parientes silvestres en el territorio nacional, por lo que no se permite la liberación de maíz genéticamente modificado en dichas áreas. Adicionalmente en el anexo III se establecen las medidas generales de protección del maíz, que incluye entre otras las siguientes: medidas sobre conocimiento, información y monitoreo, mediadas para la protección y conservación de la diversidad genética de los maíces nativos y sus parientes silvestres; dichos instrumentos regulatorios son tomados en cuenta por la Sagarpa para la resolución de solicitudes de liberación al ambiente de maíz genéticamente modificado, lo anterior en concordancia con el principio precautorio establecido en el artículo 13, fracción II, de la multicitada ley.
En todos los permisos otorgados se realizó la evaluación de riesgos correspondiente, se contó con la autorización del organismo genéticamente modificado experimentado por la Secretaría de Salud, así como el dictamen vinculante de la Secretaría de Medio Ambiente y Recursos Naturales; a cada uno se les determinó medidas de bioseguridad específicas con la finalidad de prevenir, reducir y mitigar los posibles riesgos que pudieran ocasional a la sanidad vegetal, animal y acuícola así como al medio ambiente y la diversidad biológica.
Ahora bien, para resolver una solicitud de permiso de liberación al ambiente de maíz genéticamente modificado, se considera en todo momento el enfoque metodológico de “paso a paso”, el cual indica que todo organismo genéticamente modificado que está destinado a ser liberado comercialmente debe ser previamente sometido a pruebas satisfactorias conforme a los estudios de riesgo, a la evaluación de riesgos y 1ós reportes de resultados aplicables.
También sé realiza una evaluación individual de “caso por caso”, sustentada en la evidencia científica y técnica disponible, considerando entre otros aspectos, el organismo receptor, el área de liberación y las características de la modificación genética, así como los antecedentes sobre la realización de actividades los organismos genéticamente modificados y los beneficios comparados con opciones tecnológicas alternas.
Con el marco normativo descrito, bajo los criterios establecidos en la multicitada ley y su reglamento, durante el periodo 2008-2012, la Sagarpa, a través del Senasica, ha resuelto 434 solicitudes de permisos de liberación al ambiente de organismos genéticamente modificados, de las cuales 46 fueron negativas (27 para el cultivo de maíz, 13 para el algodón, 3 para soya, 1 para trigo y 2 para canola) y 388 en sentido favorable para una superficie permitida de 1,922,092 hectáreas para los cultivos citados.
Asimismo, para el caso del maíz se otorgaron 193 permisos (168 en liberación experimental y 25 en programa piloto) en una superficie permitida de 3,452 hectáreas. En el caso del algodón se otorgaron 136 permisos (78 en liberación experimental, 53 en programa piloto y 5 en liberación comercial) en una superficie de 1,522,679 hectáreas. Para soya se emitieron 23 permisos (14 en liberación experimental, 8 en programa piloto y 1 en liberación comercial) en una superficie permitida de 3.9 hectáreas. Actualmente se encuentran en análisis y dictamen las primeras 6 solicitudes de permiso de liberación comercial de maíz genéticamente modificado con pretendida liberación en los estados de Sinaloa y Tamaulipas, en una superficie de 1,400,000 y 1,093,852 hectáreas, respectivamente.
Adicionalmente, a nivel nacional el Senasica, a partir del año 2010, implementó el Programa Anual de Monitoreo de Organismos Genéticamente Modificados de origen vegetal, el cual tiene por objeto vigilar el correcto cumplimiento de la Ley de Bioseguridad de Organismos Genéticamente Modificados a través de las actividades de monitoreo de organismos genéticamente modificados de manera aleatoria en las diferentes regiones agrícolas del territorio nacional, para detectar liberaciones no permitidas, ya sea intencionales o accidentales de estos organismos; para ello se toman muestras de tejido vegetal de los cultivos de maíz, algodón, trigo y soya y se analizan en el Centro Nacional de Referencia en Detección de Organismos Genéticamente Modificados del Senasica, con el fin de prevenir riesgos a la sanidad del país, de conformidad con la multicitada ley y su reglamento.
Hago propicia la ocasión para enviarle un cordial saludo.
Atentamente
Maestra Maricela Lecuona González (rúbrica)
Directora General Jurídica
De la diputada Lázara Nelly González Aguilar
Palacio Legislativo de San Lázaro, a 18 de septiembre de 2013.
Diputado Ricardo Anaya Cortés
Presidente de la Mesa Directiva
Cámara de Diputados
Presente
Estimado Presidente:
Por este conducto y con fundamento en lo dispuesto por el artículo 62 de la Constitución Política de los Estados Unidos Mexicanos, y lo estipulado en el capítulo III, artículo 6, sección primera, numeral 1, fracción XVI, y el capítulo IV, artículo 12, numeral 1, fracción III, del Reglamento de la Cámara de Diputados, me permito solicitar licencia por tiempo indefinido , para separarme de mis funciones legislativas como diputada federal de la LXII Legislatura del Congreso de la Unión, mismo que he venido desempeñando desde el 1 de septiembre de 2012, dicha licencia la solicito a partir del 26 de septiembre de 2013.
Sin otro particular de momento, y agradeciendo de antemano su atención me es grato quedar como su atenta y segura servidora.
Atentamente
Diputada Lázara Nelly González Aguilar (rúbrica)